Explore Any Narratives
Discover and contribute to detailed historical accounts and cultural stories. Share your knowledge and engage with enthusiasts worldwide.
David Bennett przeżył dwa miesiące z bijącym w jego klatce piersiowej sercem świni. Zmarł w marcu 2022 roku, ale jego przypadek nie był porażką. Był sygnałem. Przez dekady ksenotransplantacja – przeszczep narządów międzygatunkowych – była granicą nauki, której nie śmiano przekroczyć. Dziś ta granica znika. W laboratoriach od Bostonu po Kanton genetycznie zmodyfikowane świnie rosną, by ratować życie. Ich serca, nerki, płuca i wątroby są testowane z rezultatami, które jeszcze pięć lat temu brzmiały jak science fiction. To nie jest już pytanie „czy”, ale „kiedy”.
Historia medycyny pełna jest momentów, w których śmiała idea zderza się z upartą biologią. Ksenotransplantacja przez większość XX wieku należała do tej drugiej kategorii. Próby przeszczepów od małp kończyły się katastrofą immunologiczną w ciągu minut. Organizm człowieka rozpoznawał obcą tkankę i niszczył ją z brutalną skutecznością. Przełom nie przyszedł z kosmosu, ale z chlewu. Świnia okazała się nieoczekiwanym, idealnym kandydatem. Jej narządy są zbliżonej wielkości, fizjologia podobna, a czas ciąży krótki. Problemem były nie tyle różnice anatomiczne, co molekularne – cukrowe znaczniki na powierzchni komórek, które dla ludzkiego układu odpornościowego są jak czerwona płachta.
Prawdziwa rewolucja rozpoczęła się wraz z precyzyjnymi narzędziami do edycji genów, przede wszystkim CRISPR-Cas9. To one pozwoliły naukowcom nie tylko wyłączyć geny odpowiedzialne za te niebezpieczne antygeny, ale także wstawić do świnskiego genomu ludzkie geny, które działają jak kamuflaż. Powstały organizmy hybrydowe, biotechnologiczne arcydzieła hodowane w sterylnych warunkach. Mówimy o liniach, takich jak świnie 10 GE z dziesięcioma modyfikacjami: czterema wyłączonymi genami świni i sześcioma dodanymi genami człowieka. Jedna z zaawansowanych linii ma nawet 69 takich zmian.
„To może być przełom w transplantologii, który zmieni jej oblicze” – mówi prof. Małgorzata Czyż z Uniwersytetu Medycznego w Łodzi. „Ksenoprzeszczep nerki od genetycznie zmodyfikowanej świni to nie jest odległa przyszłość. To rzeczywistość, która dzieje się na naszych oczach w wiodących ośrodkach na świecie”.
Eksperymentalne procedury na pacjentach ze śmiercią mózgu potwierdziły, że koncepcja działa. W Chinach w 2024 roku po raz pierwszy przeszczepiono człowiekowi wątrobę od miniaturowej świni rasy Bama, zmodyfikowanej w sześciu genach. W tym samym roku w USA pacjentka Lisa Pisano, cierpiąca na zaawansowaną niewydolność serca i nerek, otrzymała najpierw sztuczne serce, a następnie nerkę od świni. Przeżyła. Te pojedyncze przypadki są jak pierwsze kroki na Księżycu – niezwykle ryzykowne, kosztowne, ale otwierające zupełnie nową drogę.
Prawdziwym poligonem doświadczalnym dla ksenotransplantacji są jednak badania na naczelnych. To tam testuje się długoterminowe przeżycie narządów. Dziecięcy Szpital w Los Angeles (Children's Hospital Los Angeles) ustanowił niepobity rekord. Jego zespół przeszczepił pawianom serca świń rasy Yucatan. Jeden z tych organów bił w ciele biorcy przez 620 dni – prawie dwa lata. To nie był szczęśliwy traf. Na czternaście przeprowadzonych transplantacji, osiem funkcjonowało przez wiele miesięcy. Kluczem okazała się kombinacja zaawansowanej inżynierii genetycznej dawcy i nowego leku immunosupresyjnego – tegoprubartu.
W przypadku ludzi rekordy są krótsze, ale równie znaczące. W kwietniu 2024 roku media obiegła wiadomość o pacjencie w USA, który przeżył z nerką świni 271 dni. To nowy rekord. Wcześniej głośno było o pacjentce Looney, której przeszczepiona nerka funkcjonowała przez 130 dni. Te liczby nie są abstrakcyjne. Dla osób spędzających lata na dializach, każde dodatkowe 100 dni z funkcjonującą nerką to dar nie do przecenienia.
„Ksenotransplantacje nie skończą się na zastawkach. To jest droga do pełnych, żywych narządów” – przekonuje prof. Tomasz Schwarz z Uniwersytetu Jagiellońskiego. „Musimy pamiętać o etyce badań na zwierzętach, ale musimy też widzieć cel: ratowanie ludzkiego życia. To jest konieczność dla współczesnej medycyny”.
Najbardziej zaskakujące postępy dotyczą płuc – narządu niezwykle delikatnego i podatnego na odrzucenie. Zespół naukowców z Chin, którego badania opublikowało pismo „Nature Medicine”, przeszczepił genetycznie zmodyfikowane płuca świni rasy Bama Xiang biorcy ze śmiercią mózgu. Organ funkcjonował przez 216 godzin – dziewięć dni – bez oznak nadostrego odrzutu. To kamień milowy dla tysięcy chorych na mukowiscydozę czy idiopatyczne włóknienie płuc, dla których jedyną szansą jest przeszczep.
Za każdym rekordem, za każdą modyfikacją genetyczną, stoi ludzka historia. Często jest to historia desperacji. David Bennett nie kwalifikował się do przeszczepu ludzkiego serca. Jego wybór był prosty: pewna śmierć albo eksperymentalna procedura z szansą na kilka dodatkowych tygodni życia. Wybrał to drugie. Jego decyzja otworzyła furtkę dla kolejnych pacjentów.
Po drugiej stronie stoi naukowiec, jak prof. Muhammad Mohiuddin z University of Maryland School of Medicine, który całą karierę poświęcił badaniom nad ksenotransplantacją serca. Jego zespół przygotowywał zabieg Bennetta przez lata. To praca pełna niepewności, presji i etycznych dylematów. Jak daleko można się posunąć? Gdzie jest granica między innowacją a lekkomyślnością? Finansowanie takich badań to dziesiątki milionów dolarów, a każda porażka jest głośna i bolesna.
I wreszcie trzecia postać: etyk. Czy mamy prawo hodować zwierzęta wyłącznie po to, by stały się źródłem części zamiennych dla ludzi? Zwolennicy argumentują, że robimy to od wieków – dla mięsa, skóry, pracy. Przeciwnicy widzą w tym redukcję istoty żywej do fabryki narządów, niebezpieczne przekroczenie kolejnej granicy. Spór jest gorący, a w tle wciąż słychać echo nieudanych przeszczepów serc od szympansów w latach 60., które zraziły opinię publiczną na dekady.
Mimo to, pęd nauki jest nie do powstrzymania. Niedobór narządów to kryzys globalny. W samej Polsce w kolejce do przeszczepu czeka stale około 1500 osób. Co dzień ktoś umiera, nie doczekawszy się dawcy. Ksenotransplantacja oferuje rozwiązanie radykalne: nieograniczone, na żądanie źródło organów. To właśnie ta ekonomiczna i humanitarna matematyka napędza badania. Nie chodzi o to, by zastąpić przeszczepy od ludzi, ale by stworzyć dla nich realną alternatywę, która skróci kolejki i da szansę tym, którzy dziś jej nie mają.
Co dalej? Eksperci, tacy jak ci zaangażowani w program 10 GE, szacują, że rutynowe przeszczepy nerek od świń mogą stać się rzeczywistością w ciągu najbliższych dziesięciu lat. Pierwsze będą to procedury dla pacjentów wysokiego ryzyka, bez innych opcji. Sukcesy, jak ten pacjenta z 271 dniami, pokazują, że nie jest to mrzonka. Jego historia jest szczególna z jeszcze jednego powodu – po przeszczepie nie wymagał izolacji w sterylnym środowisku. Żył względnie normalnie. To drobny, ale niezwykle ważny szczegół. Mówi, że przyszłość ksenotransplantacji może nie być futurystycznym koszmarem, ale po prostu kolejną, skuteczną metodą leczenia.
Historia ksenotransplantacji to długa i często bolesna saga, naznaczona zarówno naukowymi porażkami, jak i moralnymi dylematami. Przez dekady, od lat 60. do 90. XX wieku, nieudane próby przeszczepiania narządów od małp, jak choćby głośny przypadek Baby Fae w 1984 roku, która przeżyła z sercem pawiana zaledwie 21 dni, rzucały cień na całą dziedzinę. Te wczesne eksperymenty, choć tragiczne, unaoczniły fundamentalny problem: niekontrolowaną, hiperostrą reakcję odrzucenia immunologicznego, która niszczyła przeszczep w ciągu kilku minut lub godzin. Było jasne, że bez gruntownej zmiany podejścia, ksenotransplantacja pozostanie w sferze medycznych fantazji.
Prawdziwa zmiana paradygmatu nastąpiła, gdy w centrum uwagi badaczy znalazły się świnie. Nie małpy naczelne, ale właśnie świnie, okazały się idealnymi dawcami ze względu na podobieństwo anatomiczne narządów do ludzkich oraz szybki cykl reprodukcyjny, co ułatwiało hodowlę. Problemem pozostawały jednak bariery genetyczne. Dopiero rewolucja w inżynierii genetycznej, zapoczątkowana przez technologię CRISPR-Cas9 w latach 2015-2020, umożliwiła precyzyjne manipulacje genetyczne. To właśnie wtedy zaczęto usuwać geny odpowiedzialne za produkcję antygenów alfa-gal, które były głównym celem ataku ludzkiego układu odpornościowego, oraz dodawać ludzkie geny regulujące układ dopełniacza, chroniące przeszczep przed zniszczeniem.
„Ksenotransplantacja, rozumiana jako przeszczepianie tkanek lub narządów pomiędzy przedstawicielami różnych gatunków, była przedmiotem badań od wielu lat” — czytamy w przeglądzie naukowym „Kosmos. Problemy nauk i społeczeństwa” z 2023 roku. „Jednak dopiero postęp w modyfikacjach genetycznych zwierząt dawców pozwolił na realne perspektywy kliniczne”.
Ten historyczny kontekst jest kluczowy, by zrozumieć, dlaczego obecne osiągnięcia, takie jak przeżycie Davida Bennetta Sr. przez dwa miesiące z sercem świni w 2022 roku, są postrzegane jako przełomowe. Nie był to odosobniony przypadek; w listopadzie 2021 roku wszczepiono nerkę świni pacjentowi ze śmiercią mózgu na NYU Langone. Choć Lawrence Faucette, pacjent, który w 2023 roku otrzymał nerkę świni, zmarł po 40 dniach, a Richard Slayman w 2024 roku po 58 dniach, każdy taki przypadek dostarcza bezcennych danych. Te, z pozoru krótkie, okresy przeżycia są niczym innym jak świadectwem, że bariera hiperostrego odrzucenia została pokonana. To nie są porażki, ale kolejne szczeble w drabinie postępu.
Kierunek badań w ksenotransplantacji ewoluuje dynamicznie. Początkowo skupiono się na sercach i nerkach, które są stosunkowo „prostsze” pod względem immunologicznym. Jednak obecne trendy wskazują na rozszerzenie zakresu na bardziej skomplikowane i wrażliwe narządy, takie jak płuca i wątroby. W 2024 roku w Kantonie w Chinach, wątroba świni została przeszczepiona zmarłemu pacjentowi i funkcjonowała przez 10 dni, filtrując krew bez powstawania skrzepów. To było niezwykłe osiągnięcie, zważywszy na złożoność funkcji wątroby i jej kluczową rolę w metabolizmie i krzepnięciu krwi.
Jeszcze bardziej ambitne są próby z płucami. Płuca, z ich rozległą powierzchnią wymiany gazowej i bezpośrednim kontaktem ze środowiskiem zewnętrznym, są niezwykle podatne na odrzucenie i infekcje. Raporty biotechnologiczne z przełomu listopada 2025 i stycznia 2026 roku mówią o eksperymentalnym wszczepieniu lewego płuca świni pacjentowi z zachowanym własnym prawym płucem. Taki zabieg pozwala na bezpośrednie porównanie funkcji obu narządów i monitorowanie reakcji immunologicznej w kontrolowanych warunkach. Czy to nie jest kwintesencja naukowego heroizmu – balansowanie na krawędzi, by zyskać wiedzę ratującą życie?
„Świnie są idealne – rosną szybko, mają podobne narządy, litery genów można edytować” — wyjaśnia dr David Cooper z University of Alabama w wywiadzie dla „Nature” w 2024 roku. Jego słowa podkreślają pragmatyczne podejście do wyboru dawcy, które jest fundamentem sukcesu współczesnej ksenotransplantacji.
Firmy biotechnologiczne, takie jak Revivicor i eGenesis, są na pierwszej linii frontu tej rewolucji. Produkują one genetycznie zmodyfikowane świnie, które są pozbawione 10 lub więcej proimmunogennych genów, a jednocześnie posiadają ludzkie geny antyodrzutowe. Świnie GalSafe, zatwierdzone przez FDA do spożycia przez ludzi już w 2020 roku, są obecnie adaptowane jako potencjalne źródła narządów. W 2023 roku w Polsce opublikowano badania dotyczące GMO-świń jako dawców, co świadczy o globalnym zasięgu tych wysiłków. Czy to nie jest fascynujące, jak daleko zaszliśmy od prymitywnych przeszczepów, bazując na pogłębionej wiedzy o biologii molekularnej?
Liczby nie kłamią. Według danych HRSA z 2025 roku, w USA ponad 100 000 osób czeka na liście oczekujących na przeszczep narządu, a średnio 17 osób umiera każdego dnia, nie doczekawszy się pomocy. Globalnie, szacuje się, że nawet 100 milionów ludzi potrzebuje narządów. Te statystyki stanowią potężny impet dla rozwoju ksenotransplantacji. Firma eGenesis optymistycznie przewiduje, że do 2030 roku możliwe będzie wyprodukowanie miliona narządów rocznie, co całkowicie zrewolucjonizowałoby system opieki zdrowotnej.
Jednakże, jak każda innowacja o tak fundamentalnym znaczeniu, ksenotransplantacja budzi kontrowersje. Krytycy wskazują na potencjalne ryzyko zoonoz, czyli przeniesienia wirusów świńskich, takich jak PERVs (porcine endogenous retroviruses), na ludzi. Pytanie, czy świński CMV przyczynił się do śmierci Davida Bennetta, pozostaje otwarte po autopsji z 2022 roku. Istnieje również brak długoterminowych danych dotyczących przeżywalności pacjentów – większość dotychczasowych prób nie przekroczyła 6 miesięcy. Nawet rekordowe przeżycia serc świń w małpach, wynoszące 945 dni w 2022 roku na Uniwersytecie Maryland, choć imponujące, to wciąż nie są ludzkie warunki.
Etyczne aspekty również są przedmiotem burzliwych debat. Czy moralnie dopuszczalne jest hodowanie zwierząt inteligentnych, takich jak świnie, wyłącznie w celu pozyskiwania ich narządów? Organizacje takie jak PETA aktywnie sprzeciwiają się tym praktykom, oskarżając naukowców o „dehumanizację” zwierząt. Z drugiej strony, zwolennicy argumentują, że ratowanie ludzkiego życia przewyższa te zastrzeżenia, zwłaszcza w obliczu cierpienia milionów chorych. W 2025 roku Unia Europejska zakazała wykorzystywania GMO-świń do transplantacji, co pokazuje, jak zróżnicowane są podejścia regulacyjne na świecie. Gdzie leży granica, kiedy życie ludzkie jest stawką?
Mimo tych wyzwań, przyszłość ksenotransplantacji wydaje się nieuchronna. FDA rozważa komercyjne zatwierdzenia do 2027 roku. To oznacza, że to, co jeszcze niedawno było domeną fantastyki naukowej, staje się coraz bardziej realną perspektywą. Należy jednak pamiętać, że każdy postęp wymaga ostrożności, transparentności i ciągłej refleksji etycznej. Tylko w ten sposób ksenotransplantacja może faktycznie stać się zbawieniem, a nie kolejnym, kontrowersyjnym rozdziałem w historii medycyny.
Znaczenie ksenotransplantacji wykracza daleko poza laboratoryjne rekordy i pojedyncze, heroiczne operacje. To nie jest tylko kolejna technika chirurgiczna. To fundamentalna zmiana w samym paradygmacie transplantologii, przejście od modelu opartego na tragicznym darze od zmarłego dawcy do modelu medycyny spersonalizowanej i „na żądanie”. Wpływ tej zmiany będzie miał konsekwencje kulturowe, ekonomiczne i etyczne, porównywalne chyba tylko z wprowadzeniem antybiotyków. Kiedy źródło narządów przestaje być rzadkością, cały system opieki zdrowotnej musi zostać przebudowany. Kolejki znikną. Kryteria kwalifikacji mogą się poszerzyć. Medycyna zyska narzędzie, które teoretycznie może wyeliminować jedną z głównych przyczyn zgonów na świecie – niewydolność organów.
Historycznie, transplantologia zawsze była zakładniczką przypadku i tragedii. Ksenotransplantacja proponuje przejście od filozofii „daru” do filozofii „produkcji”. To rodzi niepokój, ale też niesie niewyobrażalną nadzieję. W Chinach, gdzie w 2024 roku przeprowadzono pionierski przeszczep wątroby, oraz w USA, gdzie Agencja Żywności i Leków (FDA) rozważa komercyjne zatwierdzenia do 2027 roku, widać dwa różne modele wdrażania tej technologii. Jeden bardziej eksperymentalny i odważny, drugi ostrożny i regulowany. Który okaże się skuteczniejszy? To pytanie zdefiniuje globalną mapę dostępu do tej terapii w nadchodzących dekadach.
„David Bennett przeżył dwa miesiące z bijącym w jego klatce piersiowej sercem świni. Był sygnałem” — analizuje Bartłomiej Swama, ekspert biotechnologii. Ta trafna obserwacja oddaje sedno: śmierć pacjenta nie przekreśla technologii, a jedynie wyznacza kolejny punkt na krzywej uczenia się. Każdy taki sygnał jest analizowany, a wnioski z niego napędzają kolejne iteracje badań.
Dziedzictwo, które już teraz buduje ksenotransplantacja, to coś więcej niż postęp chirurgii. To dowód na siłę interdyscyplinarnej współpracy: genetyków, immunologów, chirurgów, etyków i bioinżynierów. Firmy takie jak eGenesis czy Revivicor nie są już startupami z pogranicza fantazji; stają się integralną częścią przemysłu farmaceutyczno-biotechnologicznego. Ich praca ma szansę przekształcić transplantologię z dziedziny medycyny wysoce specjalistycznej w terapię bardziej rutynową, choć wciąż skomplikowaną. To zmienia również pozycję pacjenta – z biernego petenta w kolejkach w aktywnego uczestnika pionierskich badań klinicznych, który podejmuje świadome, choć trudne ryzyko.
Entuzjazm musi być jednak chłodzony zdrowym sceptycyzmem. Pomijanie wad i ograniczeń tej technologii byłoby poważnym błędem dziennikarskim i naukowym. Pierwszym i najpoważniejszym zarzutem pozostaje ryzyko zoonoz. Świnie, mimo modyfikacji, są rezerwuarem endogennych retrowirusów (PERVs), które mogą aktywować się w organizmie biorcy. Chociaż technologia CRISPR pozwala na dezaktywację wielu z nich, pełna gwarancja bezpieczeństwa wymaga dziesięcioleci obserwacji. Śmierć Davida Bennetta, choć oficjalnie przypisana wielu czynnikom, wciąż pozostawia pytania o możliwy udział nieznanej infekcji wirusowej. Czy jesteśmy gotowi zaakceptować ryzyko wybuchu nowej, nieprzewidywalnej pandemii, której źródłem mogłyby być przeszczepione narządy?
Kolejna wątpliwość dotyczy długoterminowej funkcjonalności ksenoprzeszczepów. Nawet jeśli unikniemy ostrego odrzutu, co z przewlekłym? Jak świnskie naczynia krwionośne, serce czy nerki zniosą dziesięciolecia pracy w obcym, ludzkim organizmie, pod ciągłym ostrzałem leków immunosupresyjnych? Dotychczasowe rekordy, nawet te sięgające 271 dni dla nerki czy 945 dni dla serca w małpie, są dalekie od gwarancji 10- czy 20-letniego przeżycia przeszczepu. Możemy stworzyć narząd, który nie zostanie odrzucony jutro, ale czy przetrwa on próbę czasu?
Aspekt etyczny również nie znika. Hodowla świń w sterylnych, izolowanych warunkach, wyłącznie jako źródła „części zamiennych”, budzi głęboki sprzeciw części społeczeństwa i filozofów. To redukcja istoty żywej do roli fabryki narządów, co dla wielu jest nie do zaakceptowania, niezależnie od celu. Regulacje prawne pozostają niejednolite i chaotyczne – podczas gdy USA idą do przodu, Unia Europejska w 2025 roku utrzymuje zakaz wykorzystywania GMO-świń do transplantacji. To tworzy niebezpieczną nierównowagę i może prowadzić do „turystyki transplantacyjnej” do krajów o łagodniejszych przepisach, ze wszystkimi jej negatywnymi konsekwencjami.
Patrząc w przyszłość, nie trzeba zgadywać. Kalendarz najbliższych lat jest już wypełniony konkretnymi punktami zwrotnymi. Do 2027 roku oczekuje się decyzji FDA dotyczącej pierwszych komercyjnych, choć wciąż warunkowych, zatwierdzeń dla ksenoprzeszczepów nerek. To otworzy drzwi do szerszych badań klinicznych fazy III. W 2025 i 2026 roku spodziewane są publikacje pełnych wyników dotyczących przeszczepów płuc świni, które obecnie są na etapie raportów wstępnych. Te dane pokażą, czy ten najbardziej wrażliwy narząd może stać się trwałym elementem portfolio ksenotransplantacji.
W Polsce i Europie kluczowy będzie rok 2026, kiedy to zapewne powróci debata nad dostosowaniem prawa do szybko rozwijającej się technologii. Czy Unia Europejska złagodzi swoje stanowisko, widząc sukcesy za oceanem? Równolegle, w Chinach należy spodziewać się dalszych, śmielszych prób z wątrobą i sercem, prawdopodobnie na większej grupie pacjentów. Przewiduję, że do końca tej dekady będziemy mieli do czynienia nie z pojedynczymi przypadkami, ale z kilkoma równoległymi programami klinicznymi na świecie, które dostarczą wystarczającej ilości danych, by oddzielić nadzieję od hype'u.
Ostateczny obraz nie jest więc ani utopijny, ani dystopijny. To obraz medycyny, która zderza się z własnymi granicami i próbuje je przesunąć za pomocą narzędzi, które sama stworzyła. Wracając do tego zimowego dnia w styczniu 2022, gdy serce świni zaczęło bić w klatce piersiowej Davida Bennetta, wiemy już, że nie był to koniec historii, ale jej bardzo wyraźny początek. Dźwięk tego bicia, monitorowany przez zespoły lekarzy, stał się rytmem, do którego dostraja się teraz cała dziedzina transplantologii. Cisza, która nastąpiła po dwóch miesiącach, nie była ciszą porażki, ale głęboką, wymowną pauzą – przed kolejnym, odważniejszym taktem.
Podsumowując, przypadek Davida Bennetta dowodzi, że ksenotransplantacja przestaje być science fiction, a staje się realną nadzieją na rozwiązanie kryzysu niedoboru narządów. Czy jesteśmy gotowi zaakceptować tę rewolucję i wspierać jej rozwój, by ocalać tysiące istnień?
Your personal space to curate, organize, and share knowledge with the world.
Discover and contribute to detailed historical accounts and cultural stories. Share your knowledge and engage with enthusiasts worldwide.
Connect with others who share your interests. Create and participate in themed boards about any topic you have in mind.
Contribute your knowledge and insights. Create engaging content and participate in meaningful discussions across multiple languages.
Already have an account? Sign in here

MIT’s 2026 breakthroughs reveal a world reshaped by AI hearts, gene-edited embryos, and nuclear-powered data centers, wh...
View Board
Samsung Galaxy S26 Ultra wprowadza rewolucyjny wyświetlacz Privacy Display, który aktywnie blokuje podglądanie ekranu po...
View Board
Des chercheurs dévoilent un transistor synaptique qui détecte le mouvement en 100 µs, ouvrant la voie à une vision IA to...
View Board
Descubra 150 anos de inovação que transformaram o telefone fixo no smartphone moderno. Conheça toda a história tecnológi...
View Board
Sebastian Will e sua equipe revolucionam a computação quântica com um disco de 3,5 mm que usa 360.000 pinças ópticas par...
View Board
Sentinel-6B wystartował 17 listopada 2025, by z precyzją do 1 cm monitorować 90% oceanów, kontynuując 30-letni rekord po...
View Board
CRISPR sta riscrivendo il destino genetico, da malattie rare a terapie personalizzate, ma solleva interrogativi etici e ...
View Board
KI-Wearables 2026 revolutionieren die Medizin: Präzisionsdiagnostik in Echtzeit, Edge-AI analysiert Vitaldaten direkt am...
View Board
Krebskristalle im All: Medizinischer Quantensprung in Schwerelosigkeit Ein hellgrauer Punkt. Winzig, fast unscheinbar a...
View Board
Archäologen entdecken auf Sulawesi eine 67.800 Jahre alte Handstencil – die älteste bekannte menschliche Kunst, die euro...
View Board
Die Berliner Mauer, 155 km Beton und Stacheldraht, trennte Familien, lässt Fluchtversuche scheitern, wurde 1989 zum Symb...
View Board
Głęboko pod ziemią detektor LZ przez 417 dni szukał ciemnej materii, ale zamiast niej odkrył neutrina ze Słońca z rekord...
View Board
L'écran et l'âme : le dilemme numérique de la santé mentale Mars 2024. Dans un cabinet parisien, une patiente décrit à ...
View Board
L'IA révolutionne la découverte de médicaments, compressant des années de recherche en mois, réduisant les coûts et ouvr...
View Board
Plongez dans l'horreur préhistorique avec "Code Violet" sur PS5, où Violet Sinclair affronte des dinosaures intelligents...
View Board
Vinte anos após o Katrina, o furacão que devastou Nova Orleans expôs desigualdades raciais e falhas governamentais, deix...
View Board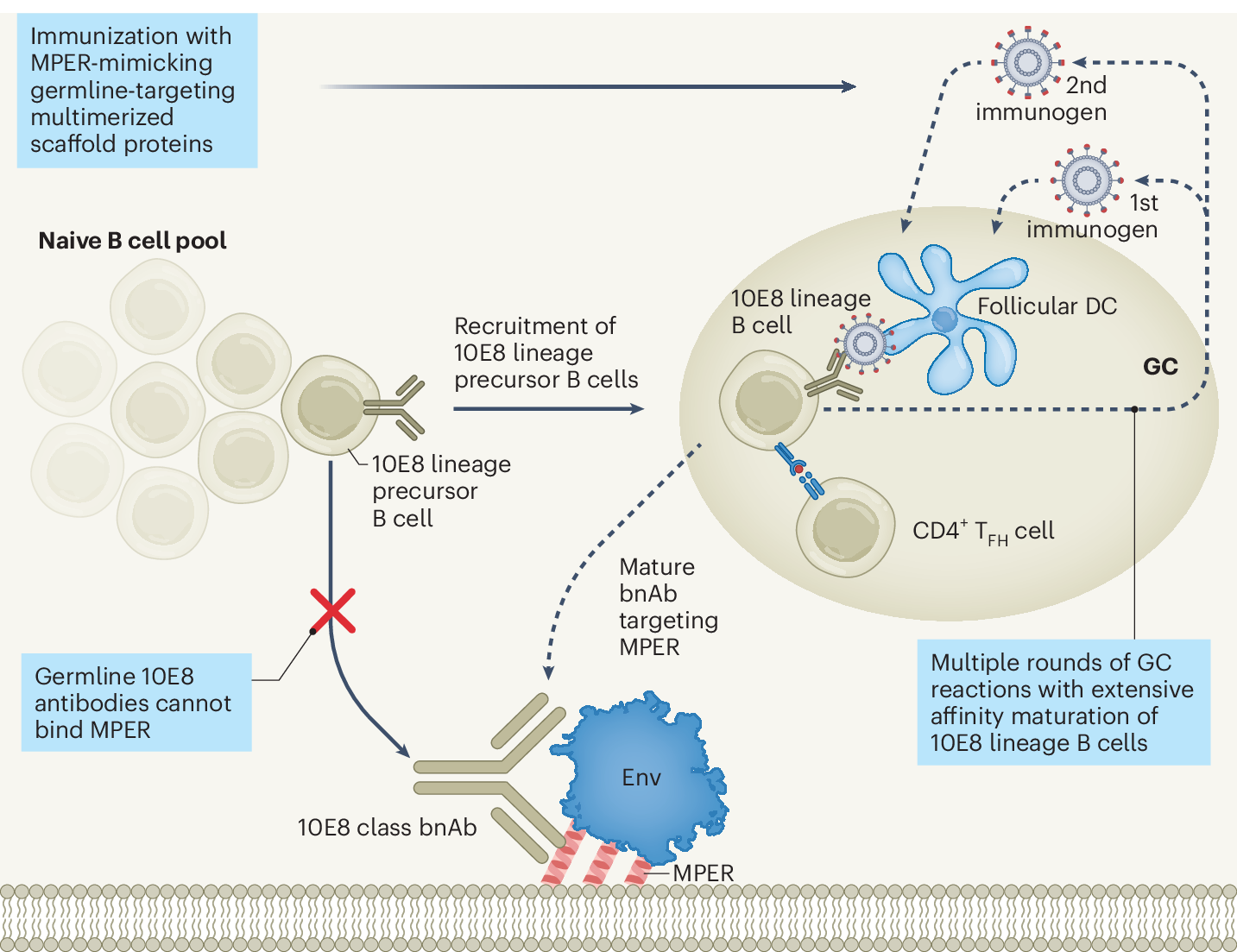
Découvrez comment les nanoparticules lipidiques LNP X ciblent les lymphocytes T CD4 pour combattre le VIH, une avancée m...
View Board
Radiation-driven wolves in Chernobyl display rapid cancer-resistant evolution, a 30-year natural experiment revealing ge...
View Board
Meta mise 2 milliards de dollars sur Manus, une startup d'IA rentable, pour dominer le marché des agents intelligents et...
View Board
Le cinéma français se réinvente en explorant de nouveaux territoires narratifs et sociaux, mêlant diversité culturelle e...
View Board
Comments