Francis Crick: El Padre de la Biología Molecular
Introducción
Francis Harry Compton Crick (1916-2004) fue un investigador británico que revolucionó el campo de la biología molecular con sus contribuciones al descubrimiento del código genético y a nuestro entendimiento de cómo se produce la vida en los seres vivos. Crick, junto con James Watson y Maurice Wilkins, recibió el Premio Nobel de Medicina en 1962 por su descubrimiento del doble hélice del ácido desoxirribo nucleico (ADN).
A lo largo de su carrera, Crick no solo fue un brillante científico sino también un pensador profundo sobre la naturaleza de la vida misma. Este artículo explorará los aspectos más significativos de la vida y obra de Francis Crick, desde su juventud hasta su legado en la ciencia moderna.
Orígenes y Formación
Francis Harry Compton Crick nació el 8 de junio de 1916 en Northampton, Inglaterra. Desde niño mostró un interés especial en la física y en el funcionamiento de la computadura humana, un tema que más tarde influiría en sus ideas sobre la mente y la inteligencia artificial.
Crick obtuvo su educación primaria en el St. Mary's Church of England School en Northampton. Durante la Segunda Guerra Mundial, Crick trabajó como ingeniero de radar en el Royal Naval Research Establishment en Portsmouth, una experiencia que le ayudaría en su futuro trabajo científico al permitirle entender el papel de las señales eléctricas en la transmisión de información.
Después de la guerra, Crick continuó sus estudios en la University of Cambridge, donde obtuvo su doctorado en biología. En su tesis doctoral, Crick estudió la cristalografía de rayos X, un campo que le proporcionaría las herramientas necesarias para investigar la estructura molecular de macromoléculas como el ADN.
Primeros Años Científicos
Tras obtener su doctorado, Crick comenzó a trabajar en el Laboratorio Nacional de Física de Alta Energía (MRC LMB) en Cambridge en 1948. Su trabajo inicial en este laboratorio se centraba en la cristalografía de rayos X, una técnica que utiliza luz para crear imágenes de la estructura interna de cristales. Esta disciplina era cruciales para entender la estructura de las proteínas y ADN, temas que se convertirían en su principal área de investigación.
Poco después de iniciar su labor en el MRC LMB, Crick se interesó por el ADN, una molécula que almacenaba el código genético de todo ser vivo. La cristalografía de rayos X proporcionaba una manera de observar la estructura de la ADN a nivel molecular, pero resultaba muy difícil obtener muestras puras de ADN en forma cristalizada.
Crick empezó a experimentar con diferentes técnicas para purificar la ADN y lograr su cristalización. Sus esfuerzos se vieron recompensados cuando logró cristalizar una cepa mutada del ADN de bacterias, lo cual fue un paso crucial en la obtención de imágenes de su estructura.
La Revolución de la Crystallization de ADN
En 1951, Maurice Wilkins comenzó a trabajar en el MRC LMB con Crick. Wilkins había sido uno de los pioneros en la cristalografía de rayos X del ADN y, junto con su colega Rosalind Franklin, habían obtenido impresionantes fotografías de cristales de ADN en bacterias.
Durante esta época, Maurice Wilkins presentó algunos de estos resultados a Crick. Estas fotografías capturaron la imagen característica del ADN y marcaron el punto de inflexión hacia la identificación de la estructura tridimensional de esta molécula.
Crick, con su experiencia en cristalografía de rayos X, comprendió rápidamente las implicaciones científicas de estas imágenes. A lo largo del curso de 1951, desarrolló teorías sobre cómo se podría estructurar el ADN en una forma tridimensional que pudiera explicar sus propiedades biológicas.
Uno de los mayores desafíos que enfrentaban Crick y Wilkins era encontrar una estructura que pudiera contener la información necesaria para codificar todos los órganismos vivos. Crick se dio cuenta que la forma tridimensional del ADN necesitaba poseer una simetría especial para guardar información genética de forma eficiente. Con esto en mente, se sumergió en una serie de cálculos matemáticos y teorías físicas para determinar qué tipo de estructura podría cumplir estas características.
Abril de 1953: La Revelación del Doble Hélice
Vinieron los momentos definitivos en abril de 1953 cuando Crick y James Watson (ex alumno de Cambridge) se unieron para completar su teoría sobre la estructura tridimensional del ADN. Watson, inspirado por el trabajo previo de Crick y el análisis cuidadoso de las imágenes de los cristales de ADN obtenidos por Franklin, finalmente sintetizó su idea de que la estructura del ADN podía ser una forma doblemente enrollada (doble hélice).
Crick, en conversación con Watson, recordó sus propias teorías previas durante una conferencia de física a principios de 1951, y estos encuentros fueron decisivos. Entre ambos, Crick y Watson elaboraron una estructura en la que la cadena de adn estaba formada por dos átomos de fósforo y dos átomos de azúcar, con las parejas de bases nitrogenadas (adenina, citosina, timina e uracilo) conectadas entre sí por pares de hidrógenos y dispuestas de forma que fueran visibles bajo la cristalografía de rayos X realizada por Franklin.
Aparte del trabajo en el MRC LMB, Crick también colaboró con otros científicos como Rosalind Franklin, quien proporcionó datos clave a través de su brillante trabajo de cristalografía de rayos X, aunque las contribuciones específicas de Franklin a la forma del doble hélice son disputadas en términos de reconocimiento por algunas partes en la comunidad científica.
El Descubrimiento y su Legado
El descubrimiento del doble hélice del ADN fue publicado simultáneamente en el Journal of Molecular Biology en abril de 1953. El documento firmado por James Watson y Francis Crick se tituló "Construction of Nucleic Acid Chains from their Atomic Precursors", describiendo brevemente cómo se podrían vincular las bases del ADN y cuál sería su estructura. Este descubrimiento cambió dramáticamente nuestro entendimiento de la forma en que la genética funcionaba y cómo el ADN contenía la información para producir proteínas, las moléculas vitales que construyen y mantienen los organismos vivos.
Crick y Watson compartieron el Premio Nobel de Fisiología o Medicina en 1962 junto con Maurice Wilkins por su "descubrimiento sobre la estructura del ADN y su importancia progresiva para el estudio de las procesos biológicos". Aunque esta distinción fue principalmente para Crick y Watson, el papel de Wilkins y, por supuesto, de Franklin fue crucial para el descubrimiento y merece consideración en la historia científica.
Obras Posteriores y Pensamientos sobre la Inteligencia Artificial
Más allá del descubrimiento del ADN, Crick se dedicó a la investigación en la neurociencia y en particular en la comprensión del problema cerebro-cognición. Trabajó durante muchos años en el Medical Research Council Unit en Cambridge, donde exploró cómo funciona la mente y cómo los seres humanos adquieren conocimientos y recuerdos.
Uno de sus trabajos más conocidos en este campo es el modelo que propuso para la memoria cortemancha, denominado "hipotelesis de la memoria progresiva". Según esta teoría, los recuerdos recientes y accesibles están guardados en un conjunto de neuronas en el hipocampo, mientras que los recuerdos menos accesibles se guardan a largo plazo en otras áreas del cerebro mediante un proceso gradual.
En los años siguientes, Crick se interesó en la conexión entre la estructura del cerebro y la función de las neuronas, y cómo éstas transmiten información en forma de impulsos eléctricos. Señaló que la inteligencia no se limita a los cerebros humanoide como los de las personas, sino que puede existir en formas más simples y en sistemas no vivos. Esto llevó a su interés en la inteligencia artificial y en particular en el desarrollo de máquinas capaces de replicar las funciones cognitivas humanas.
Conclusión
Francis Crick fue más que un científico genial; fue un visionario que cambió nuestra comprensión de la biología molecular y el funcionamiento del cerebro. Su descubrimiento del ADN marcó un antes y un después en la historia de la ciencia y sentó las bases para muchas de las investigaciones posteriores en biología y medicina. Además, sus contribuciones en el estudio de la memoria y la mente, y sus reflexiones sobre la inteligencia artificial, continúan siendo relevantes para las avances actuales en neurociencia y robótica.
La vida y obra de Crick siguen siendo ejemplo para muchos jóvenes científicos que buscan resolver problemas complejos e innovar nuevas áreas de estudio. Su pasión por la ciencia y su capacidad para conectar ideas aparentemente alejadas convirtieron a Crick en una figura influyente y respetada en la comunidad científica internacional.
En la segunda parte de este artículo exploraremos aún más profundamente la vida académica y personal de Crick, así como su legado en la ciencia moderna.
Continuación en la Segunda Parte
Para continuar leyendo sobre Francis Crick e investigar más sobre su impacto en la neurociencia y el campo de la inteligencia artificial, puedes dar clic en "Continuar leyendo la segunda parte" en nuestra sección de noticias de ciencia.
Investigaciones en la Neurociencia
Más allá de su trabajo sobre el ADN, Francis Crick continuó investigando la neurociencia durante los años siguientes. En 1988, se trasladó a la Salk Institute for Biological Studies en San Diego, California, donde continuó sus investigaciones sobre la complejidad del círculo de la memoria y la forma en que los seres humanos aprenden y recuerdan.
Un aspecto central de su investigación en la neurociencia fue la exploración de la base biológica de la mente. Crick era convencido de que el cerebro no solo procesa los datos sensoriales, sino que también almacena la información de múltiples formas, incluyendo la memoria y el pensamiento. Este enfoque se basaba en la teoría de que el cerebro y la mente son entidades inseparables, lo que llevó a la teoría del "cerebro cognitivo".
Crick y su colega Christof Koch publicaron su teoría de la cognición en 2000, propuesta que fue publicada en The Inordinate Complexity of the Brain and Mind. Según esta teoría, la cognición implica no solo el procesamiento de los estímulos sensoriales, sino también la integración de información a nivel del cerebro, lo que permite la planificación, la toma de decisiones y el aprendizaje. Crick y Koch propusieron que la memoria y la cognición se realizan a través de una red compleja de neuronas interconectadas en áreas específicas del cerebro.
Algunas de las áreas del cerebro que Crick se interesó fueron el hipocampo y la corteza neocortex, regiones clave involucradas en la formación y el almacenamiento de la memoria. Su trabajo en esta área contribuyó a entender mejor cómo las neuronas transmiten información y cómo se codifican los recuerdos a largo plazo.
Contribuciones a la Inteligencia Artificial
Francis Crick también dedicó tiempo a la investigación en la inteligencia artificial, una área que estaba en suspenso en los años 1970 y 1980. Se convirtió en uno de los principales proponentes de la idea de que la inteligencia humana no solo se basa en los procesos cognitivos, sino que también requiere la capacidad para aprender y adaptarse a nuevas situaciones.
En 1985, Crick publicó un artículo titulado "The Recent Origin of Computation by Neural Networks in the Brain" en Nature. En este trabajo, explicó cómo las conexiones neurales en el cerebro permitían la realización de cálculos y procesos de pensamiento. Estas conexiones no son estáticas, sino que cambian en respuesta a las experiencias y los estímulos. Crick se propuso que estas mismas mecánicas podrían ser reproducidas en sistemas artificiales, abriendo el camino para la inteligencia artificial.
Crick y otros investigadores se interesaron en cómo los patrones de actividad de las neuronas podían ser utilizados para crear algoritmos que imitaran la inteligencia humana. Esta visión llevó a la creación de redes neuronales artificiales, una técnica que se está utilizando ampliamente hoy en día en el procesamiento de lenguaje natural y la reconocimiento de voz.
La Cerebro-Cognición y la Memoria
Hacia la final de su carrera, Crick se volcó en las teorías del círculo de la memoria, una propuesta que sugiere que la memoria es almacenada y recodificada en varios niveles de la cerebro, no solo en una sola área del cerebro. Según esta teoría, los recuerdos iniciales son rápidamente codificados en el hipocampo, antes de ser transferidos a otras áreas del cerebro, como la corteza prefrontal, donde se almacenan a largo plazo.
Esta idea, conocida como la teoría del rechazo de la memoria, propuesta originalmente por Richard Atwood y David Glanzman, fue ampliada por Crick, que argumentó que el hipocampo no simplemente codifica los recuerdos, sino que también realiza cambios en la memoria almacenada en otras áreas del cerebro. Crick sugirió que este proceso de rechazo y reescritura de recuerdos ayuda a mantener la integridad de la memoria mientras se adapta a nuevas experiencias.
Crick también se interesó en el papel de los glías, células no nerviosas en el cerebro, en la formación y almacenamiento de la memoria. Estas células ayudan a mantener y proteger las conexiones entre las neuronas, pero también producen factores que influyen en el crecimiento y la formación de nuevas conexiones neurales. Crick creía que estas funciones de los glías son cruciales para la formación de la memoria a largo plazo.
Conferencias y Colaboraciones
A lo largo de su carrera, Crick participó en numerosas conferencias y colaboraciones internacionales con científicos de todo el mundo. Una de sus conferencias más notables fue el First Annual Conference on the Biology of Computation, en el que presentó su teoría sobre el cerebro cognitivo y la base de la inteligencia artificial. Estas conferencias no solo ayudaron a difundir sus ideas, sino también a establecer contactos importantes con otros líderes en campos relacionados.
Uno de estos contactos fue con los científicos japoneses Kazuhiko Kanda y Toshio Endo, con los cuales trabajó en la creación de un sistema de neurocomputación que imitaba la forma en que las neuronas en el cerebro procesan la información. Este trabajo llevó a la creación de redes neuronales artificiales que lograron imitar algunos aspectos del pensamiento humano y del aprendizaje.
Otra colaboración importante fue con el profesor David Hubel y el profesor Torsten Wiesel, quienes ganaron el premio Nobel de Fisiología o Medicina en 1981 por sus descubrimientos sobre la visión en el cerebro. Crick se interesó en cómo las regiones del cerebro que procesan la visión se relacionan con el resto del cerebro y cómo se codifican los recuerdos visuales. Estos trabajos sentaron los fundamentos para entender mejor cómo se almacena y utiliza la información sensorial en el cerebro.
Vida Personal y Legado
A pesar de su enfoque en la investigación científica, Crick mantuvo una vida privada y se desinteresó de las actividades académicas más convencionales. No se casó, y a lo largo de su vida, se describió como un soltero dedicado a su trabajo. Su estilo de vida era simple, y a menudo trabajaba hasta altas horas de la noche, convencido de que la ciencia requería una dedicación incesante.
Tras su retiro en 1977, Crick siguió publicando trabajos científicos y mantuvo activos contactos con colegas en todo el mundo. En 1988, tras su movimiento a San Diego, Crick continuó su investigación en el Salk Institute hasta su muerte en 2004.
Crick dejó una huella indelible en el mundo de la ciencia, no solo como uno de los principales descubridores del doble hélice del ADN, sino también como un pensador innovador que exploró la conexión entre la estructura del cerebro y la cognición. Su trabajo en la inteligencia artificial y su visión de la mente humana siguen siendo fundamentales para la neurociencia y la inteligencia artificial moderna.
En la siguiente sección, continuaremos explorando la importancia de los descubrimientos de Crick en la biología molecular y su legado para la ciencia moderna.
Continuación en la Tercera Parte
Para continuar leyendo sobre la vida, contribuciones y legado de Francis Crick, puedes dar clic en "Continuar leyendo la tercera parte" en nuestra sección de noticias de ciencia.
En la tercera parte de este artículo, exploraremos la importancia de los descubrimientos de Crick en la biología molecular y su legado para la ciencia moderna.
Impacto en la Biología Molecular y la Ciencia Moderna
La revolución genética iniciada por Crick y sus colegas ha tenido efectos duraderos en todas las áreas de la biología y la medicina. Una de las consecuencias más inmediatas fue el desarrollo de técnicas para clonar genes y secuenciar ADN, procesos que han sido cruciales para el progreso de la biología experimental y la genómica.
La secuenciación del genoma humano representó una pico de este progreso. Crick y otros científicos trabajaron incansablemente para hacer la secuencia del genoma humano posible. A medida que las técnicas para secuenciar ADN se volvían cada vez más precisas y más económicas, la cantidad de información disponible para el descubrimiento genético aumentó exponencialmente.
El proyecto del Genoma Humano, liderado por la Oficina Nacional de Salud y Servicios de Servicios Médicos de Estados Unidos y la Wellcome Trust Sanger Institute en el Reino Unido (donde trabajó Crick en sus últimos años), fue un hito significativo. Este proyecto fue fundamental no solo para el avance de la medicina genética, sino también para nuestra comprensión de las enfermedades del ADN, como los cánceres hereditarios.
Hacia una Mejor Comprensión del Cáncer
Crick siempre estuvo interesado en la biología del cáncer. Junto con otros investigadores, trabajó para entender cómo los errores en la información genética pueden llevar a la formación de tumores. Uno de sus trabajos más influyentes fue su teoría sobre el origen evolutivo del cáncer, que sugiere que el cáncer es una enfermedad evolutiva, resultado de una competencia entre tejido cancerígeno y tejido normal.
Estaría equivocado decir que las investigaciones en el cáncer se agotaron con el descubrimiento del ADN. Actualmente, muchas áreas de investigación relacionadas con el ADN y el genoma humano están centradas en el tratamiento del cáncer. Los anticuerpos monoclonales, terapias dirigidas y terapias génicas se han visto impulsadas por un mayor conocimiento del ADN y sus mutaciones asociadas.
Lucha contra la Pobreza Genómica
En su último informe importante, publicado en Nature Reviews Genetics en 2001, título "Cancer as a genetic disease", Crick enfatizó la importancia de entender completamente cómo los errores en el ADN conducen al cáncer. Argumentó que la detección y corrección temprana de los errores génicos podrían prevenir muchos casos de cáncer, reduciendo así la carga global de enfermedad en la sociedad.
Este enfoque ha llevado a la idea de la medicina personalizada, donde el conocimiento del genoma individual puede ser utilizado para predecir y prevenir enfermedades. Crick fue un precursor en la promoción de este enfoque, y su trabajo en la genómica y la bioinformática ha dejado una huella duradera en la industria farmacéutica y biotecnológica.
Conclusiones
Francis Crick fue una de las figuras más prominentes y creativas en la historia de la ciencia moderna. Dejarle su legado significa más que solo recordarlo por el descubrimiento del doble hélice del ADN y su papel en la genómica. Su pasión por la ciencia, su visión en profundidad y su capacidad para hacer conexiones insospechadas han inspirado generaciones de científicos.
Desde su muerte en 2004, Crick sigue siendo una referencia constante en el campo de la biología molecular y la neurociencia. Los avances en secuenciación de ADN, terapias génicas y bioinformática siguen avanzando gracias a sus teorías y descubrimientos.
En retrospectiva, se puede afirmar que Crick no solo cambió nuestras percepciones de cómo funciona la vida a nivel molecular, sino que también abrió nuevas puertas para una comprensión still deepening of how the brain works and how intelligence can be modeled and replicated. Su legacy extends well beyond the discovery of DNA itself, encompassing his groundbreaking work in neuroscience and his profound insights into the nature of life itself.
Por lo tanto, Crick no sólo es una figura histórica, sino también un modelo para las mentes curiosas y desafiantes del mañana. Su legado seguirá resplandeciendo como un faro para aquellos que persiguen la verdadera comprensión de la vida y cómo funciona en los seres vivos.
¿Te gustaría conocer más sobre el impacto perdurable de los descubrimientos de Francis Crick?
Para descubrir más detalles sobre cómo sus innovaciones son fundamentales para el progreso continuo en las ciencias biológicas y para entender cómo están transformando nuestra comprensión de la condición humana, puedes ver nuestros otros recursos sobre biología molecular y neurociencia.
Te esperamos en nuestra sección de noticias científicas para descubrir más!


Gregor Mendel : Le Père de la Génétique Moderne
Introduction
Gregor Mendel est une figure emblématique de la science, souvent considéré comme le père fondateur de la génétique. Ses travaux révolutionnaires sur les petits pois ont jeté les bases de la compréhension des mécanismes de l'hérédité, bien que leur importance n'ait été pleinement reconnue que des décennies après sa mort. Cet article explore la vie, les découvertes et l'héritage de ce moine et scientifique visionnaire.
Les Jeunes Années de Gregor Mendel
Johann Mendel, plus tard connu sous le nom de Gregor Mendel, est né le 20 juillet 1822 à Heinzendorf, dans l'Empire autrichien (aujourd'hui Hynčice en République tchèque). Fils d'un fermier, il a grandi dans un environnement rural où l'agriculture était au cœur de la vie quotidienne. Dès son plus jeune âge, il a développé une fascination pour la nature et les plantes, une passion qui allait influencer toute sa carrière.
Malgré les difficultés financières de sa famille, Mendel a pu poursuivre des études grâce au soutien de sa sœur et de son professeur, qui ont reconnu son intelligence et sa soif de connaissances. Après des études secondaires brillantes, il a intégré l'Institut philosophique d'Olomouc, où il a suivi des cours de philosophie, de physique et de mathématiques. Cependant, confronté à des problèmes financiers et à des enjeux familiaux, il a finalement choisi d'entrer au monastère augustinien de Brno en 1843, prenant le nom de Gregor.
La Vie Monastique et les Études Scientifiques
Au monastère Saint-Thomas de Brno, Mendel a trouvé un environnement propice à l'étude et à la réflexion. Sous la direction de l'abbé Cyrill Napp, le monastère encourageait les recherches scientifiques, notamment dans les domaines de l'agriculture et de l'horticulture. Mendel a ainsi pu combiner sa vocation religieuse avec sa passion pour les sciences naturelles.
En 1851, il fut envoyé à l'Université de Vienne pour approfondir ses connaissances en sciences. Pendant deux ans, il y étudia la botanique, la physique, la chimie et les mathématiques, des disciplines qui allaient jouer un rôle crucial dans ses futures expériences. C'est à cette époque qu'il fut initié aux travaux de scientifiques comme Doppler et Unger, qui influencèrent sa méthodologie.
Les Expériences sur les Petits Pois
De retour au monastère en 1853, Mendel commença ses célèbres expériences sur les petits pois (Pisum sativum) dans le jardin du monastère. Ces recherches, qu'il mena méticuleusement pendant huit ans (1856-1863), avaient pour but de comprendre les lois régissant la transmission des caractères héréditaires.
Mendel choisit les petits pois pour plusieurs raisons : leur cycle de croissance rapide, la facilité avec laquelle on pouvait contrôler leur pollinisation, et la présence de caractères distinctifs facilement observables (comme la couleur des graines, la texture de la peau, ou la forme des gousses). Il croisa méthodiquement différentes variétés, notant avec précision les résultats sur des milliers de plantes.
Les Lois de Mendel
De ses observations, Mendel formula trois principes fondamentaux, aujourd'hui connus sous le nom de lois de Mendel :
1. La Loi de l'Uniformité des Hybrides de Première Génération (F1)
Lorsqu'on croise deux variétés pures présentant des caractères opposés (par exemple, des graines jaunes et des graines vertes), tous les descendants de la première génération (F1) expriment un seul de ces caractères, appelé caractère dominant. L'autre caractère, dit récessif, semble disparaître.
2. La Loi de Ségrégation des Caractères
Dans la deuxième génération (F2), issue du croisement des hybrides F1, les caractères récessifs réapparaissent selon un rapport prévisible de 3 (dominant) pour 1 (récessif). Mendel en déduisit que les facteurs héréditaires (que nous appelons aujourd'hui gènes) se séparent lors de la formation des gamètes.
3. La Loi de l'Assortiment Indépendant
Les facteurs héréditaires responsables de différents caractères sont transmis indépendamment les uns des autres lors de la reproduction. Cette loi ne s'applique qu'aux gènes situés sur des chromosomes différents ou très éloignés sur un même chromosome.
La Réception des Travaux de Mendel
En 1865, Mendel présenta ses résultats à la Société des Sciences Naturelles de Brno, puis les publia l'année suivante sous le titre Recherches sur des hybrides végétaux. Malheureusement, ses travaux furent largement ignorés par la communauté scientifique de l'époque. Plusieurs raisons expliquent cet échec :
- Le langage mathématique employé par Mendel était inhabituel en biologie à cette époque, ce qui rendit son texte difficile d'accès pour beaucoup de ses contemporains.
- Ses conclusions contredisaient la théorie alors dominante de l'hérédité par mélange, selon laquelle les caractères des parents se "mélangeaient" chez les descendants.
- Peu de scientifiques s'intéressaient alors aux mécanismes de l'hérédité, domaine encore marginal dans les sciences biologiques.
Découragé par ce manque de reconnaissance, Mendel abandonna progressivement ses recherches scientifiques pour se concentrer sur ses responsabilités administratives au monastère, devenant abbé en 1868.
Les Années Suivantes et la Fin de Vie
Dans les dernières années de sa vie, Mendel s'engagea dans un conflit avec les autorités gouvernementales qui imposaient des taxes aux institutions religieuses. Cette lutte, combinée à l'indifférence face à ses travaux scientifiques, le plongea dans une certaine amertume. Il mourut le 6 janvier 1884 d'une maladie rénale chronique, sans avoir vu la reconnaissance de ses découvertes.
C'est seulement au début du XXe siècle, avec la redécouverte indépendante de ses lois par Hugo de Vries, Carl Correns et Erich von Tschermak, que l'importance fondamentale des travaux de Mendel fut enfin reconnue. Ses principes devinrent alors la pierre angulaire de la génétique moderne.
La Redécouverte des Travaux de Mendel et leur Influence sur la Science
Trois décennies après la mort de Mendel, en 1900, trois botanistes européens - Hugo de Vries aux Pays-Bas, Carl Correns en Allemagne et Erich von Tschermak en Autriche - redécouvrirent indépendamment les lois de l'hérédité que Mendel avait formulées. Cette triple redécouverte marqua le début de la reconnaissance posthume des travaux du moine tchèque et l'émergence de la génétique comme discipline scientifique à part entière.
Les raisons de cette redécouverte tardive sont multiples. À la fin du XIXe siècle, les avancées en cytologie avaient permis d'observer les chromosomes et leur comportement lors de la division cellulaire, créant un contexte plus favorable à la compréhension des mécanismes mendéliens. De plus, les scientifiques cherchaient alors des explications aux variations observées dans les espèces, ce qui les amena à revisiter les travaux antérieurs sur l'hérédité.
L'Intégration des Idées Mendéliennes dans la Science Moderne
La redécouverte des lois de Mendel coïncida avec le développement de la théorie chromosomique de l'hérédité. En 1902, Walter Sutton et Theodor Boveri firent le lien entre les "facteurs" mendéliens et les chromosomes, proposant que ces derniers étaient les supports physiques de l'hérédité. Cette synthèse entre les observations cytologiques et les principes mendéliens établit les fondations de la génétique classique.
Dans les années qui suivirent, les scientifiques commencèrent à appliquer les principes mendéliens à divers organismes, confirmant leur universalité bien au-delà des petits pois. Thomas Hunt Morgan et son équipe, travaillant sur les drosophiles, découvrirent cependant que certains gènes semblaient liés - une observation qui mena à la notion de liaison génétique et à la création des premières cartes chromosomiques.
Les Limites et les Précisations des Lois Mendeliennes
Bien que révolutionnaires, les lois de Mendel présentent certaines limites qui furent progressivement découvertes au fil des avancées scientifiques :
1. Les Exceptions à la Dominance Complète
Les premières expériences de Mendel portaient sur des traits où un allèle était complètement dominant par rapport à l'autre. Cependant, on découvrit par la suite d'autres modes d'hérédité comme :
- La dominance incomplète (phénotype intermédiaire chez les hétérozygotes)
- La codominance (expression simultanée des deux allèles)
- Les gènes létaux (allèles causant la mort lorsqu'homozygotes)
2. L'Épistasie et les Interactions Génétiques
Certains gènes peuvent en masquer l'expression d'autres, un phénomène appelé épistasie. Ces interactions complexes, où plusieurs gènes influencent un même caractère, sortent du cadre strict des lois mendéliennes simples.
3. Les Traits Polygéniques
De nombreux caractères, comme la taille ou la couleur de la peau chez l'homme, sont déterminés par l'action combinée de nombreux gènes (hérédité polygénique), aboutissant à une variation continue plutôt qu'à des catégories discrètes comme chez les petits pois de Mendel.
4. Les Gènes Liés et le Recombinaison Génétique
Les gènes situés sur un même chromosome ont tendance à être hérités ensemble, ce qui constitue une exception à la loi de l'assortiment indépendant. Toutefois, le phénomène de crossing-over pendant la méiose permet un réassortiment partiel de ces gènes liés.
L'Impact de la Génétique Mendelienne sur l'Agriculture
Les principes découverts par Mendel révolutionnèrent rapidement les pratiques agricoles et l'amélioration des plantes cultivées. Les sélectionneurs purent désormais prédire avec plus de précision les résultats des croisements et développer des variétés présentant des combinaisons désirables de caractères.
L'application des lois mendéliennes permit :
- Le développement de lignées pures pour une meilleure uniformité des cultures
- La création d'hybrides F1 présentant une vigueur hybride (hétérosis)
- La sélection plus efficace de résistances aux maladies
- L'amélioration des qualités nutritionnelles des plantes alimentaires
La Révolution Verte et ses Bases Mendeliennes
Dans les années 1960-1970, la "Révolution verte" qui transforma l'agriculture mondiale s'appuya largement sur les principes de la génétique mendélienne. Norman Borlaug et d'autres agronomes utilisèrent les techniques de sélection basées sur ces principes pour développer des variétés de céréales à haut rendement, sauvant des millions de vies de la famine.
Mendel et l'Évolution : La Synthèse Moderne
Initialement, les travaux de Mendel semblaient en contradiction avec la théorie de l'évolution de Darwin, car ils montraient une transmission discontinue des caractères alors que Darwin envisageait une variation continue. Cette apparente contradiction fut résolue avec le développement de la génétique des populations et la synthèse moderne de l'évolution dans les années 1930-1940.
Les scientifiques comme Ronald Fisher, J.B.S. Haldane et Sewall Wright démontrèrent comment les mutations discrètes des gènes mendéliens, soumises à la sélection naturelle, pouvaient conduire à l'évolution graduelle des espèces. Cette fusion des idées de Mendel et Darwin constitue encore aujourd'hui le cadre théorique principal de la biologie évolutive.
L'Héritage Culturel et Symbolique de Mendel
Au-delà de son impact scientifique, Gregor Mendel est devenu une figure emblématique dans l'histoire des sciences. Son parcours illustre plusieurs aspects importants de la recherche scientifique :
- Le rôle parfois sous-estimé de la rigueur méthodologique et de la quantification en biologie
- L'importance de la persévérance face à l'incompréhension des contemporains
- La valeur des approches interdisciplinaires (Mendel combinait biologie, mathématiques et physique)
- Le potentiel des recherches apparemment modestes (comme l'étude des petits pois) pour révolutionner la science
Les Commémorations et les Lieux de Mémoire
De nombreux lieux et institutions honorent aujourd'hui la mémoire de Mendel :
- L'abbaye Saint-Thomas de Brno, où il mena ses expériences, abrite maintenant un musée qui lui est consacré
- L'Université Mendel de Brno porte son nom
- Un cratère lunaire et l'astéroïde (3313) Mendel ont été nommés en son honneur
- Le "Mendel Day" est célébré le 20 juillet (date de sa naissance) par des institutions scientifiques
Les journaux qu'il tenait méticuleusement, ses lettres et ses notes originales sont aujourd'hui considérés comme des trésors de l'histoire des sciences, étudiés par les historiens et les généticiens pour mieux comprendre comment a émergé cette discipline fondamentale.
Mendel et les Développements Contemporains de la Génétique
L'héritage de Mendel s'étend bien au-delà de la génétique classique et trouve des échos surprenants dans les développements les plus récents de la biologie moléculaire. Les découvertes fondamentales du XXe siècle, comme la structure de l'ADN par Watson et Crick en 1953, peuvent être considérées comme des prolongements naturels du cadre conceptuel établi par Mendel un siècle plus tôt.
De la Génétique Mendelienne à la Génétique Moléculaire
La transition des "facteurs héréditaires" de Mendel aux gènes moléculaires modernes représente un des parcours intellectuels les plus fascinants de la science :
- 1909 : Wilhelm Johannsen introduit le terme "gène" pour désigner les unités mendéliennes d'hérédité
- 1941 : George Beadle et Edward Tatum formulent la théorie "un gène - une enzyme"
- 1953 : Découverte de la structure en double hélice de l'ADN
- 2003 : Achèvement du Projet Génome Humain, aboutissement spectaculaire des recherches initiées par Mendel
Les Applications Médicales des Principes Mendelians
La médecine moderne doit beaucoup aux découvertes de Mendel, particulièrement dans le domaine des maladies génétiques. La compréhension des modes de transmission héréditaire a permis :
1. Le Diagnostic et le Conseil Génétique
Les généticiens utilisent quotidiennement les lois de Mendel pour évaluer les risques de transmission des maladies héréditaires comme :
- La mucoviscidose (transmise sur le mode récessif autosomique)
- La maladie de Huntington (dominante autosomique)
- L'hémophilie (liée au chromosome X)
2. Le Développement de Thérapies Innovantes
La thérapie génique, bien que complexe, s'appuie sur des principes fondamentaux établis par Mendel. Les progrès récents comme CRISPR-Cas9, une technologie d'édition génomique, permettent aujourd'hui d'envisager la correction directe des gènes défectueux - une perspective qui aurait semblé inimaginable à l'époque de Mendel.
Les Débats Éthiques Issus des Découvertes Mendeliennes
L'héritage scientifique de Mendel soulève d'importantes questions éthiques que la société doit affronter :
1. Le Dépistage Génétique et la Vie Privée
La capacité à prédire les risques de développer certaines maladies pose des questions complexes concernant :
- Le droit à ne pas connaître son statut génétique
- La confidentialité des données génétiques
- Les discriminations possibles par les assureurs ou employeurs
2. L'Ingénierie Génétique et ses Limites
Les techniques permettant de modifier directement le génome humain, comme CRISPR, ouvrent des perspectives thérapeutiques importantes mais soulèvent aussi des inquiétudes quant aux dérives eugénistes potentielles.
La Pédagogie Mendelienne et son Évolution
L'enseignement des lois de Mendel constitue toujours une introduction fondamentale à la génétique, bien que les approches pédagogiques aient considérablement évolué :
1. Du Petit Pois aux Modèles Virtuels
Alors que Mendel travaillait avec de vrais plants de pois, les étudiants d'aujourd'hui peuvent :
- Utiliser des simulateurs informatiques de croisements génétiques
- Explorer des banques de données génomiques
- Visualiser en 3D la structure des protéines codées par les gènes
2. La Réhabilitation des Aspects Historiques
Les historiens des sciences ont récemment mis en lumière plusieurs aspects méconnus des travaux de Mendel :
- Son usage innovant des statistiques en biologie
- Ses échanges intellectuels avec d'autres scientifiques de son époque
- Ses expériences moins connues sur les abeilles et d'autres plantes
Perspectives Futures : Au-Delà de Mendel?
Au XXIe siècle, la génétique s'est considérablement complexifiée, révélant des phénomènes que Mendel n'aurait pu anticiper :
1. L'Épigénétique : Une Hérédité Non-Mendelienne
Les mécanismes épigénétiques, qui modifient l'expression des gènes sans changer la séquence d'ADN, ajoutent une couche de complexité aux principes mendéliens classiques.
2. Le Microbiome et l'Hérédité Holobiontique
La reconnaissance du rôle des microbiotes dans la santé humaine introduit des formes d'hérédité qui transcendent la simple transmission des gènes parentaux.
3. La Génétique des Populations à l'Ère Génômique
Les études d'association pangénomique (GWAS) permettent aujourd'hui d'analyser simultanément des milliers de variations génétiques à l'échelle de populations entières.
Conclusion : L'Immortalité Scientifique de Gregor Mendel
Plus de 150 ans après ses expériences fondatrices, Gregor Mendel reste une figure centrale de la biologie. Son travail illustre plusieurs leçons intemporelles :
- L'importance des observations minutieuses et de la quantification rigoureuse
- La valeur des modèles biologiques simples pour découvrir des principes universels
- La persistance nécessaire pour défendre des idées nouvelles
- L'interconnexion profonde entre les différentes disciplines scientifiques
Aujourd'hui, alors que la génétique se trouve au cœur des plus grandes avancées médicales et biotechnologiques, le cadre conceptuel établi par ce moine visionnaire continue de guider les chercheurs. Son héritage ne se limite pas à trois lois simples, mais réside surtout dans l'esprit scientifique rigoureux et novateur qu'il a incarné - un esprit qui reste essentiel pour relever les défis scientifiques du XXIe siècle.
Comme Mendel dans son jardin de Brno, les scientifiques d'aujourd'hui continuent à chercher des modèles dans la complexité du vivant, prouvant que les grandes découvertes peuvent parfois germer dans les endroits les plus inattendus et à partir des travaux les plus modestes en apparence.
Har Gobind Khorana : Un Pionnier de la Biologie Moléculaire
Les Débuts d'un Esprit Brillant
Har Gobind Khorana naquit le 9 janvier 1922 dans le petit village de Raipur, situé dans l'actuel Pakistan. Issu d'une famille modeste, il grandit dans un environnement où l'éducation était considérée comme un privilège. Malgré les difficultés financières, son père, un percepteur d'impôts, encouragea vivement l'éducation de ses enfants. Cette détermination familiale permit à Khorana de développer très tôt une passion pour les sciences.
Son parcours académique débuta à l'Université du Pendjab à Lahore, où il obtint son baccalauréat en 1943 et sa maîtrise en 1945. Ses résultats exceptionnels lui valurent une bourse du gouvernement indien pour poursuivre ses études au Royaume-Uni. En 1948, il obtint son doctorat en chimie organique à l'Université de Liverpool, marquant ainsi le début d'une carrière scientifique remarquable.
Une Carrière Scientifique Internationale
Après son doctorat, Khorana effectua des recherches postdoctorales en Suisse à l'École polytechnique fédérale de Zurich, où il travailla avec le professeur Vladimir Prelog, futur lauréat du prix Nobel. Cette expérience enrichissante lui permit d'approfondir ses connaissances en chimie organique et de développer des compétences qui s'avérèrent cruciales pour ses futures découvertes.
En 1952, Khorana partit pour le Canada, où il occupa un poste à l'Université de la Colombie-Britannique. C'est là qu'il commença à s'intéresser à la biochimie et plus particulièrement aux acides nucléiques. Ses recherches sur la synthèse des nucléotides et des oligonucleotides attirèrent l'attention de la communauté scientifique internationale.
En 1960, Khorana rejoignit l'Institut de recherche en enzymes de l'Université du Wisconsin-Madison aux États-Unis. Ce fut dans ce prestigieux institut qu'il réalisa ses travaux les plus marquants, ceux qui allaient révolutionner notre compréhension du code génétique et lui valoir le prix Nobel de physiologie ou médecine en 1968.
La Révolution du Code Génétique
Les travaux les plus célèbres de Khorana portèrent sur le décryptage du code génétique et la synthèse artificielle de gènes. En collaboration avec Marshall Nirenberg et Robert Holley, il élucida la manière dont les séquences d'ADN déterminent la structure des protéines. Plus précisément, Khorana démontra comment les nucléotides de l'ARN messager (ARNm) sont organisés en triplets (codons) qui spécifient chaque acide aminé dans une protéine.
Une de ses contributions majeures fut la synthèse du premier gène artificiel en 1970. Cette prouesse technique ouvrit la voie au développement du génie génétique et de la biotechnologie moderne. Khorana et son équipe réussirent à synthétiser un gène d'ARN de transfert de levure, démontrant qu'il était possible de créer artificiellement des séquences d'ADN fonctionnelles.
Méthodologie et Innovations Techniques
Khorana développa plusieurs techniques révolutionnaires pour la synthèse des acides nucléiques. Parmi ses innovations les plus importantes figurent :
- La méthode de synthèse des oligonucleotides par voie chimique, qui permit la création de séquences d'ADN définies
- L'utilisation de polymérases pour assembler des oligonucleotides en gènes complets
- Le développement de systèmes enzymatiques pour étudier la réplication de l'ADN
Ces méthodes devinrent des outils fondamentaux pour la biologie moléculaire et sont encore largement utilisées aujourd'hui dans les laboratoires du monde entier.
Reconnaissance et Prix Nobel
En 1968, Khorana reçut le prix Nobel de physiologie ou médecine, conjointement avec Marshall Nirenberg et Robert Holley, pour leur interprétation du code génétique et sa fonction dans la synthèse des protéines. Cette reconnaissance couronna des années de recherche intensive et marqua un tournant dans l'histoire de la biologie moléculaire.
Outre le Nobel, Khorana reçut de nombreuses autres distinctions prestigieuses, dont le Prix Albert Lasker pour la recherche médicale fondamentale en 1968 et la National Medal of Science en 1987. Il fut élu membre de plusieurs académies scientifiques prestigieuses, dont la National Academy of Sciences des États-Unis et la Royal Society de Londres.
Un Héritage Scientifique Durable
Les découvertes de Khorana ont eu un impact profond sur de nombreux domaines scientifiques et médicaux. Elles ont permis :
- Le développement des techniques de séquençage de l'ADN
- L'avènement de la biotechnologie et des thérapies géniques
- Une meilleure compréhension des maladies génétiques
- Les progrès en médecine personnalisée
Son travail sur la synthèse des gènes ouvrit également la voie à la création d'organismes génétiquement modifiés et à la production industrielle de protéines thérapeutiques comme l'insuline humaine.
Khorana fut non seulement un scientifique brillant mais aussi un mentor dévoué. Tout au long de sa carrière, il forma de nombreux étudiants et chercheurs qui continuèrent à faire progresser le domaine de la biologie moléculaire. Son approche rigoureuse et sa créativité scientifique continuent d'inspirer les générations actuelles de chercheurs.
Les années de maturité et les contributions ultérieures
Après ses découvertes révolutionnaires sur le code génétique, Har Gobid Khorana continua à faire progresser la science avec la même passion et la même rigueur. En 1970, il accepta un poste prestigieux au Massachusetts Institute of Technology (MIT), où il devint professeur de biologie et de chimie. Ce nouvel environnement stimulant lui permit d'approfondir ses recherches et d'explorer de nouvelles voies scientifiques.
Les travaux sur les membranes biologiques
Dans les années 1970, Khorana se tourna vers l'étude des membranes biologiques, un domaine alors en plein essor. Il s'intéressa particulièrement aux protéines membranaires, ces structures complexes qui jouent un rôle crucial dans de nombreux processus cellulaires. Son équipe se concentra sur la bactériorhodopsine, une protéine membranaire présente dans certaines bactéries photosynthétiques.
Les recherches de Khorana sur la bactériorhodopsine permirent de mieux comprendre comment cette protéine agit comme une pompe à protons, convertissant l'énergie lumineuse en énergie chimique. Ces travaux eurent des implications importantes pour la compréhension des mécanismes de la vision et de la photosynthèse. Ils ouvrirent également de nouvelles perspectives sur le fonctionnement des protéines membranaires en général.
La synthèse des gènes et ses applications
Parallèlement à ses travaux sur les membranes, Khorana continua à perfectionner les techniques de synthèse des gènes. Dans les années 1980, son laboratoire mit au point des méthodes plus efficaces pour assembler des fragments d'ADN synthétique. Ces avancées techniques permirent d'accélérer considérablement le processus de synthèse génétique et de réduire les coûts associés.
L'une des applications les plus marquantes de ces techniques fut la production de protéines recombinantes. Khorana et son équipe utilisèrent des gènes synthétiques pour produire des protéines thérapeutiques comme l'insuline humaine et l'hormone de croissance. Ces travaux contribuèrent directement au développement de l'industrie biotechnologique naissante.
L'enseignement et la transmission du savoir
Khorana ne fut pas seulement un chercheur exceptionnel, mais aussi un enseignant dévoué. Au MIT, il forma des générations d'étudiants et de chercheurs qui allaient à leur tour faire progresser la biologie moléculaire. Son approche pédagogique était basée sur la rigueur expérimentale et la créativité scientifique.
De nombreux témoignages de ses anciens étudiants décrivent Khorana comme un mentor patient et exigeant, toujours prêt à guider ses élèves vers l'excellence. Il insistait sur l'importance de bien comprendre les principes fondamentaux avant de se lancer dans des expériences complexes. Cette philosophie éducative influença profondément la formation de nombreux scientifiques de premier plan.
Les collaborations scientifiques
Bien qu'il ait souvent travaillé de manière indépendante, Khorana collabora avec plusieurs autres scientifiques de renom. Parmi ses collaborations les plus fructueuses figurent ses travaux avec le biochimiste Gobind Khorana et le généticien Marshall Nirenberg. Ces partenariats scientifiques permirent d'accélérer les découvertes sur le code génétique et ses applications.
Khorana encourageait également la collaboration interdisciplinaire, travaillant avec des chimistes, des physiciens et des informaticiens pour résoudre des problèmes biologiques complexes. Cette approche ouverte et collaborative devint un modèle pour la recherche scientifique moderne.
Les défis et les obstacles
Malgré ses succès, la carrière de Khorana ne fut pas sans difficultés. Comme de nombreux scientifiques immigrés, il dut faire face à des défis culturels et professionnels en s'installant aux États-Unis. Les premières années furent particulièrement difficiles, avec des problèmes de financement et d'intégration dans le milieu académique américain.
Sur le plan scientifique, Khorana rencontra également des obstacles techniques importants dans ses recherches. La synthèse des gènes dans les années 1960 et 1970 était un processus extrêmement laborieux, nécessitant des mois de travail pour produire de courtes séquences d'ADN. Khorana et son équipe durent développer des méthodes innovantes pour surmonter ces difficultés techniques.
La reconnaissance tardive
Bien que ses travaux aient été rapidement reconnus par la communauté scientifique, Khorana dut attendre plusieurs années avant de recevoir la pleine reconnaissance de ses pairs. Certains de ses concepts les plus avancés, comme l'utilisation des gènes synthétiques en biotechnologie, ne furent pleinement appréciés que des années plus tard.
Cette reconnaissance tardive n'affecta cependant pas la détermination de Khorana à poursuivre ses recherches. Il continua à travailler avec la même passion jusqu'à la fin de sa carrière, explorant toujours de nouvelles frontières scientifiques.
L'héritage scientifique continu
Les découvertes de Khorana continuent d'influencer la science moderne de multiples façons. Les techniques de synthèse génétique qu'il a développées sont aujourd'hui à la base de toute la biotechnologie moderne. Sans ses travaux pionniers, des domaines comme la génomique ou la médecine personnalisée n'auraient pas pu se développer aussi rapidement.
De nombreuses techniques actuelles, comme la PCR (Polymerase Chain Reaction) ou l'édition génomique CRISPR, s'appuient sur des principes que Khorana a contribué à établir. Son héritage est particulièrement visible dans les domaines suivants :
- La production de médicaments biotechnologiques
- La thérapie génique
- La biologie synthétique
- La recherche sur les maladies génétiques
Les laboratoires du monde entier continuent d'utiliser des méthodes dérivées de ses travaux originaux, témoignant de l'impact durable de ses contributions scientifiques.
Les honneurs et distinctions
Au cours de sa longue carrière, Khorana reçut de nombreux prix et distinctions en reconnaissance de ses contributions à la science. Parmi les plus prestigieux, on peut citer :
- Le Prix Nobel de physiologie ou médecine (1968)
- Le Prix Albert Lasker (1968)
- La National Medal of Science (1987)
- Le Prix Louisa Gross Horwitz (1968)
- Le Prix Gairdner (1980)
Il fut également élu membre de plusieurs académies scientifiques prestigieuses, dont la National Academy of Sciences des États-Unis, la Royal Society de Londres et l'Académie des sciences indienne. Ces reconnaissances témoignent de l'estime dans laquelle la communauté scientifique tenait ses travaux.
仔Les dernières années et l'héritage durable
Dans les dernières décennies de sa vie, Har Gobind Khorana continua à travailler activement dans son laboratoire, malgré son âge avancé. Il maintint un intérêt constant pour les développements scientifiques, en particulier dans le domaine de la biologie moléculaire. Jusqu'à la fin, il resta un observateur attentif des progrès technologiques et théoriques dans son domaine de prédilection.
Une vie dédiée à la science
Khorana passa ses dernières années à Cambridge, Massachusetts, entouré de sa famille et de ses collègues. Même après sa retraite officielle du MIT en 2007, il continua à conseiller des étudiants et à participer à des séminaires scientifiques. Son esprit vif et sa passion pour la recherche ne faiblirent jamais, témoignant d'une curiosité intellectuelle qui dura toute sa vie.
Le 9 novembre 2011, Har Gobind Khorana s'éteignit à l'âge de 89 ans, laissant derrière lui un héritage scientifique immense. Sa mort fut largement commémorée dans le monde scientifique, avec de nombreux hommages rendus par ses pairs et ses anciens étudiants. Les journaux scientifiques du monde entier publièrent des nécrologies soulignant l'importance de ses contributions à la biologie moderne.
L'influence sur les générations futures
L'impact de Khorana sur la science ne se limite pas à ses propres découvertes. Il a également influencé des générations de scientifiques à travers son enseignement et son mentorat. De nombreux chercheurs qui ont travaillé dans son laboratoire sont devenus à leur tour des leaders dans leurs domaines respectifs, perpétuant ainsi son approche rigoureuse et créative de la recherche.
Les méthodes qu'il a développées continuent d'être enseignées dans les universités du monde entier, formant la base de la formation en biologie moléculaire. Ses manuels et publications restent des références pour les étudiants et les chercheurs, témoignant de la clarté de sa pensée et de son talent pour expliquer des concepts complexes.
L'actualité de ses découvertes
Plus de cinquante ans après ses découvertes majeures, les travaux de Khorana restent étonnamment pertinents. Les techniques de synthèse génétique qu'il a développées ont évolué, mais les principes fondamentaux restent les mêmes. Aujourd'hui, avec l'avènement de la biologie synthétique et de l'ingénierie génétique, ses travaux trouvent de nouvelles applications dans des domaines qu'il n'aurait pu imaginer.
La médecine personnalisée, la thérapie génique, la production de biocarburants - toutes ces technologies de pointe s'appuient sur les fondations posées par Khorana et ses contemporains. Son rêve d'utiliser la connaissance du code génétique pour améliorer la santé humaine est en train de devenir réalité grâce aux avancées récentes en génomique et en biotechnologie.
Les défis éthiques
Les découvertes de Khorana ont également soulevé des questions éthiques importantes sur l'utilisation des technologies génétiques. Comme il l'avait lui-même reconnu, le pouvoir de manipuler le code génétique vient avec une grande responsabilité. Les débats actuels sur l'édition génétique, le clonage et la modification génétique des organismes trouvent leurs racines dans les travaux pionniers de Khorana et de ses collègues.
Bien qu'il n'ait pas vécu pour voir les développements les plus récents comme CRISPR, Khorana avait anticipé bon nombre des dilemmes éthiques auxquels nous sommes confrontés aujourd'hui. Ses réflexions sur la responsabilité des scientifiques restent une référence dans les discussions sur l'éthique en biotechnologie.
Un héritage qui perdure
L'héritage de Har Gobind Khorana est multiple. Scientifiquement, il a révolutionné notre compérhension du code génétique et ouvert la voie à la biotechnologie moderne. Humainement, il a montré comment la persévérance et l'intégrité peuvent mener à des découvertes transformatrices. Socialement, son parcours d'immigrant devenu lauréat du prix Nobel reste une source d'inspiration pour les jeunes scientifiques du monde entier.
De nombreuses institutions et prix portent aujourd'hui son nom, perpétuant sa mémoire. Le Khorana Program, par exemple, est un programme d'échange scientifique entre l'Inde et les États-Unis qui encourage les jeunes chercheurs. Des laboratoires, des bourses et des conférences scientifiques honorent régulièrement sa mémoire, témoignant de l'estime durable dont il jouit dans la communauté scientifique.
Une inspiration pour les générations futures
L'histoire de Khorana - celle d'un jeune homme issu d'un village modeste devenu l'un des plus grands scientifiques du XXe siècle - continue d'inspirer. Elle rappelle que la science n'a pas de frontières et que les grandes découvertes peuvent venir des endroits les plus inattendus. Son parcours montre aussi l'importance de soutenir l'éducation et la recherche, où que ce soit dans le monde.
Pour les jeunes scientifiques, particulièrement ceux issus de milieux défavorisés, Khorana reste un modèle de ce qu'il est possible d'accomplir avec de la détermination et une passion pour la connaissance. Son héritage le plus durable est peut-être cette inspiration qu'il continue de fournir aux générations futures de chercheurs.
Conclusion
Har Gobind Khorana fut l'un des grands architectes de la biologie moléculaire moderne. Ses découvertes fondamentales sur le code génétique ont changé à jamais notre compréhension de la vie. Plus qu'un simple scientifique, il fut un visionnaire dont les travaux continuent de façonner la science et la médecine contemporaines.
Son parcours exceptionnel, de son enfance dans un petit village indien à son ascension vers les plus hautes sphères de la science mondiale, témoigne du pouvoir transformateur de l'éducation et de la recherche. Aujourd'hui, alors que nous entrons dans l'ère de la biologie synthétique et de la médecine génomique, l'héritage de Khorana est plus vivant que jamais.
Comme il l'a lui-même dit un jour : "La science est une aventure sans fin vers l'inconnu." Har Gobind Khorana fut l'un des plus grands explorateurs de cette aventure, et ses découvertes continueront d'éclairer le chemin des générations futures de scientifiques.
Walter Gilbert: Pionero de la Biología Molecular
Introducción: un visionario en la ciencia
Walter Gilbert, nacido el 21 de marzo de 1932 en Boston, Massachusetts, es un científico cuyo trabajo ha dejado una huella indeleble en el campo de la biología molecular. Reconocido por su papel en el desarrollo de métodos para descifrar el código genético, Gilbert ganó en 1980 el Premio Nobel de Química junto a Paul Berg y Frederick Sanger. Su contribución fue esencial para el avance en la comprensión del ADN y la base molecular de los organismos vivos. Con una carrera que abarca desde la física teórica hasta la política científica, Gilbert es una figura inspiradora cuyas iniciativas han trascendido laboratorios y aulas.
De la física teórica a la biología molecular
Antes de devenir en una celebridad de la biología molecular, Walter Gilbert inició su formación académica en las áreas de la física y las matemáticas. Completó su licenciatura en Química y Física en la Universidad de Harvard en 1953, y posteriormente, obtuvo un doctorado en Física Matemática en 1957 en la misma institución. Su incursión en la biología fue el resultado de su interés por resolver los problemas fundamentales de la vida, lo cual lo llevó a cambiar el rumbo de su carrera hacia la bioquímica.
Este cambio de disciplina no fue sencillo y requirió que Gilbert aprendiera de manera autodidacta sobre biología molecular en un momento en que el campo todavía se encontraba en sus primeras etapas. Sin embargo, su sólida base en ciencias exactas le proporcionó las herramientas necesarias para abordar los problemas biológicos desde una perspectiva analítica y revolucionaria.
Descifrando el código genético: el Método de Gilbert
Una de las contribuciones más significativas de Walter Gilbert al campo de la biología molecular fue el desarrollo de un método innovador para secuenciar el ADN. En colaboración con Allan Maxam, Gilbert ideó un método químico para determinar la secuencia de bases en moléculas de ADN. Este avance, conocido como el "Método Maxam-Gilbert", fue una de las primeras técnicas prácticas para la secuenciación de ADN, y proporcionó una base sobre la cual se desarrollaron técnicas posteriores más avanzadas.
El Método Maxam-Gilbert involucraba la fragmentación química selectiva del ADN en segmentos más pequeños, cuya secuenciación se lograba mediante la identificación de las terminales de estos fragmentos. Aunque eventualmente fue reemplazado por métodos más eficientes y seguros, como el método de Sanger, su impacto en su época fue revolucionario, permitiendo a los científicos explorar la estructura genética de forma más detallada.
Impacto en la industria y la academia
Además de su logro en la decodificación del ADN, Walter Gilbert ha sido un influyente defensor de la aplicación del conocimiento científico en el ámbito comercial. Fue cofundador de Biogen, una de las primeras compañías biotecnológicas en explotar el potencial de la ingeniería genética. Su visión era que los avances en la biología molecular podían traducirse en prácticas médicas innovadoras y tratamientos más efectivos para las enfermedades.
Como académico, Gilbert mantuvo una posición destacada en la Universidad de Harvard, donde desempeñó un papel crucial tanto en la enseñanza como en la investigación. Su presencia en el campus no solo fomentó un ambiente de investigación interdisciplinaria, sino que también inspiró a nuevas generaciones de científicos a explorar el vasto potencial de la biología molecular.
El legado de un Nobel
Cuando recibió el Premio Nobel de Química en 1980, la comunidad científica reconoció un legado que no solo se encontraba en sus descubrimientos, sino también en su capacidad para inspirar a otros. A través de sus esfuerzos, Gilbert contribuyó a sentar las bases de modernas técnicas genómicas que hoy impulsan la medicina y la biotecnología. Su enfoque interdisciplinario y su habilidad para integrar teoría con experimentación son ejemplos de cómo la ciencia puede progresar cuando se cruzan los límites tradicionales de las disciplinas académicas.
Entre sus múltiples honores y premios, Walter Gilbert también ha sido miembro de varias academias y sociedades científicas de renombre, demostrando así su estatura como uno de los pioneros del siglo XX en la biología molecular. Su trabajo sigue siendo una fuente de inspiración y es a menudo citado por científicos que buscan expandir las fronteras del conocimiento genético y molecular.
Desafíos y controversias en el auge de la biotecnología
A pesar de sus logros significativos, la carrera de Walter Gilbert no estuvo exenta de desafíos y controversias. En la década de 1980, el auge de la biotecnología generó un intenso debate ético y social sobre la manipulación genética y sus implicaciones. Gilbert, como defensor ferviente de la investigación genética, se encontró en el centro de estas discusiones. Abogó fuertemente por el uso de la biotecnología en aplicaciones médicas y agrícolas, subrayando su potencial para mejorar la calidad de vida y alimentar a una población mundial en crecimiento.
Sin embargo, este entusiasmo no siempre fue compartido por la opinión pública o incluso por todos sus colegas científicos. Las preocupaciones sobre la seguridad y los posibles efectos no deseados de la ingeniería genética llevaron a un llamado a la regulación estricta. Gilbert, aunque consciente de estos riesgos, defendió la importancia del progreso científico junto con un enfoque ético y responsable. Para él, la ciencia debía avanzar sin miedo, pero con responsabilidad, balanceando innovación con cautela.
La contribución de Gilbert a la ciencia educativa
Más allá de sus logros en el ámbito de la investigación, Walter Gilbert también dejó una impresión duradera en la educación científica. A lo largo de su carrera, enfatizó la importancia de un enfoque multidisciplinario en la enseñanza, integrando la biología con la física, la química y las matemáticas. Su pasión por la enseñanza inspiró a muchos de sus estudiantes, quienes posteriormente hicieron contribuciones significativas en diversos campos de la ciencia.
Gilbert fue un firme defensor de la necesidad de reformar la educación científica para adaptarse a los rápidos cambios en el conocimiento tecnológico y biológico. Abogó por currículos que no solo enseñaran los fundamentos científicos, sino que también fomentaran el pensamiento crítico y la capacidad de resolver problemas complejos. Este estímulo hacia un enfoque integral en la educación ayudó a preparar a las futuras generaciones de científicos para los desafíos que plantean los avances biotecnológicos contemporáneos.
Innovaciones continuas y sus aportaciones al proyecto Genoma Humano
Durante la década de 1990, Walter Gilbert se involucró activamente en el Proyecto Genoma Humano, un esfuerzo internacional masivo destinado a mapear la secuencia completa del genoma humano. Este proyecto monumental prometía revolucionar nuestra comprensión de la genética humana y proporcionar una base para avances médicos futuros. Gilbert, cuya carrera se estableció sobre la comprensión del material genético, aportó su vasta experiencia y conocimiento a este ambicioso esfuerzo.
El Proyecto Genoma Humano no solo fue un hito científico, sino que también generó nuevas preguntas éticas y sociales sobre la privacidad genética y la potencial discriminación basada en la información genética. Gilbert, consciente de estos problemas, participó en discusiones sobre cómo regular el uso de la información del genoma de manera que se maximicen sus beneficios y se minimicen sus riesgos. Su participación subrayó una vez más su compromiso con la integración de la ética en el avance científico.
El faro de la ciencia en tiempos de incertidumbre
En tiempos de incertidumbre, cuando los avances tecnológicos traen consigo tanto promesas como preocupaciones, figuras como Walter Gilbert se destacan como faros de conocimiento y claridad. Su vida y carrera reflejan la evolución de un periodo en el que la biología molecular y la biotecnología emergen como fuerzas dominantes que ponen en jaque el estado del conocimiento previamente aceptado.
En sus frecuentes apariciones públicas y conferencias, Gilbert comparte no solo su conocimiento técnico, sino también su visión de una ciencia en equilibro con la sociedad. Al desafiar los límites de lo que es posible, siempre abogó por un enfoque prudente, reflejado en su insistencia por la educación científica robusta y políticas reglamentarias sólidas. Por ello, su legado no viene solo de descubrimientos técnicos, sino también, y quizás más significativamente, de fomentar una cultura de respeto y responsabilidad dentro de la esfera científica.
Walter Gilbert sigue siendo una figura clave cuya influencia atraviesa el tiempo, invitando constantemente a la comunidad científica a reflexionar sobre el papel crucial que el conocimiento puede y debe desempeñar en la mejora de la humanidad. Sus contribuciones no solo han redefinido una disciplina, sino que han proporcionado un marco de referencia para la innovación futura con conciencia y propósito.
La visión emprendedora y el liderazgo en la biotecnología
Además de sus contribuciones académicas y científicas, Walter Gilbert también destacó como un pionero empresarial en el sector de la biotecnología. Su cofundación de Biogen en 1978 fue un paso audaz que marcó el camino para la comercialización de la investigación genética. Biogen se convirtió en una de las empresas más influyentes en el desarrollo de terapias innovadoras para diversas enfermedades, impulsadas por grandes avances en ingeniería genética.
La visión de Gilbert para Biogen no solo incluía el desarrollo de nuevos tratamientos, sino también la creación de un puente entre el mundo académico y la industria. Creyó fervientemente que los descubrimientos científicos no deberían quedarse confinados a los laboratorios, sino que deberían encontrar aplicaciones prácticas que beneficien a la sociedad en general. Bajo su liderazgo, Biogen no solo prosperó económicamente, sino que también estableció un modelo para futuras empresas biotecnológicas que buscaban llevar los avances científicos al mercado.
El impacto filosófico y ético de su trabajo
A lo largo de su carrera, Gilbert no se limitó solamente a los aspectos técnicos de la biología molecular y la biotecnología. También se preocupó profundamente por las implicaciones filosóficas y éticas de sus descubrimientos y aplicaciones. Como defensor del debate ético en la ciencia, promovió continuamente la reflexión sobre cómo los avances en genómica afectaban los conceptos fundamentales de identidad y naturaleza humana.
Walter Gilbert abordó estos temas no solo en círculos académicos, sino también en el ámbito público, abogando por una conversación abierta sobre los límites y alcances de la manipulación genética. Su enfoque era inclusivo, alentando a científicos, filósofos y ciudadanos a participar juntos en el diálogo sobre el futuro de la humanidad en la era biotecnológica. Esta perspectiva ayudó a preparar a la sociedad para enfrentar los retos morales que acompañan a los progresos científicos.
Legado duradero y homenaje a un científico visionario
El legado de Walter Gilbert perdura a través de sus innumerables contribuciones al mundo científico y a la industria biotecnológica, así como por su impacto educativo y ético. Su habilidad para anticipar y moldear el futuro de la biología molecular lo ha consolidado como un científico visionario cuyos logros continúan influyendo en la investigación y la innovación en todo el mundo.
En reconocimiento a sus contribuciones, ha sido homenajeado con numerosas distinciones y premios a nivel internacional. Su trabajo ha sido un recordatorio constante del poder transformador de la ciencia cuando se la aborda con integridad y dedicación. Los reconocimientos, sin embargo, no son solo un testimonio de su genio, sino también del espíritu colaborador y del lucro sostenible que promovió a lo largo de su carrera.
Conclusiones: Walter Gilbert y el futuro de la ciencia
Al mirar hacia el futuro, la influencia de Walter Gilbert en la biología molecular se hace aún más relevante en un mundo donde la biotecnología sigue experimentando un crecimiento sin precedentes. Las herramientas que perfeccionó y los modelos que desarrolló siguen siendo la base de gran parte de la investigación actual, incluidas las tecnologías emergentes como la edición genética CRISPR.
En un contexto donde el potencial de transformación de estas tecnologías es inmenso, la perspectiva de Gilbert sobre la ciencia como un esfuerzo responsable y ético es más pertinente que nunca. Su legado es una guía para aquellas futuras generaciones de científicos que deberán balancear la innovación con la cautela y el respeto hacia los principios éticos fundamentales.
En resumen, Walter Gilbert no solo cambió el curso de la biología molecular y la biotecnología, sino que también sentó las bases para un enfoque de la ciencia que aboga por un mejor entendimiento de la vida en armonía con los valores humanos. Su vida y obra continúan inspirando a aquellos que trabajan en la frontera de lo conocido, siempre en busca de la verdad a través de la curiosidad, el rigor y una profunda sensibilidad hacia el impacto de la ciencia en la sociedad.

Barbara McClintock: La Científica que Revolucionó la Genética
Una Vida Dedicada a la Ciencia
Barbara McClintock es una figura prominente en el ámbito de la genética, conocida por su trabajo pionero en el estudio de los elementos transponibles o "genes saltarines". Su vida y carrera científica están llenas de logros notables y desafíos que logró superar, dejando un legado que sigue influyendo en la investigación actual.
McClintock nació en 1902 en Hartford, Connecticut, y creció en Brooklyn, Nueva York. Su interés por la ciencia fue evidente desde una edad temprana, lo que la llevó a estudiar en la Universidad de Cornell, donde obtuvo su doctorado en botánica en 1927. Durante su tiempo en Cornell, desarrolló un interés profundo por la genética, un campo que en ese momento se encontraba en un estado incipiente y lleno de potencial.
Contribuciones Significativas a la Genética
El trabajo de McClintock en genética fue revolucionario, especialmente su descubrimiento de elementos transponibles en el maíz en la década de 1940. Estos son segmentos de ADN que pueden moverse a diferentes posiciones dentro del genoma de una célula, un concepto radical en ese momento. Antes de sus descubrimientos, se asumía que los genes ocupaban localizaciones fijas en los cromosomas. La idea de que los genes podrían saltar y causar mutaciones o cambios en las características de un organismo fue inicialmente recibida con escepticismo.
A pesar de la resistencia de la comunidad científica, McClintock siguió adelante con su investigación. Su enfoque meticuloso y observaciones detalladas la llevaron a comprender cómo estos elementos transponibles podían influir en la expresión genética y la estabilidad del genoma. Estas conclusiones sentaron las bases para una nueva comprensión de la genética, influyendo en estudios sobre variabilidad genética, evolución y enfermedades.
Reconocimientos y Legado
A lo largo de su carrera, McClintock recibió numerosos premios y honores, culminando con el Premio Nobel de Fisiología o Medicina en 1983. Fue la primera mujer en recibir este galardón de manera individual, un reconocimiento a la magnitud de su trabajo en un período en que las mujeres científicas a menudo eran pasadas por alto. Este logro destacó la importancia de su descubrimiento y consolidó su lugar en la historia de la ciencia.
Su legado perdura no solo en la genética sino también en la forma en que su perseverancia y dedicación a la ciencia han inspirado a generaciones de investigadores. El impacto de sus descubrimientos se extiende a diversas áreas de la biología, influyendo en el desarrollo de la biotecnología y la comprensión de enfermedades genéticas complejas.
Un Espíritu Cautivado por el Misterio del ADN
McClintock se caracterizó por su pasión inquebrantable por la ciencia, su curiosidad insaciable y su capacidad para ver más allá de lo aparentemente obvio. Trabajó en un momento en que no existían las herramientas modernas de la biología molecular, dependiendo de su excepcional habilidad observacional para hacer descubrimientos que cambiaron la forma en que comprendemos la herencia genética.
Su vida refleja cómo la dedicación y un enfoque innovador pueden superar la duda y el escepticismo de las instituciones científicas establecidas. McClintock era conocida por su habilidad para trabajar sola, y a menudo se sumergía en semanas de trabajo solitario en el laboratorio, siguiendo las pistas que otros descartarían. Esta tenacidad fue esencial en un momento en que sus teorías eran vistas con desdén por ser consideradas demasiado especulativas.
Contribuyó no solo al avance del conocimiento científico, sino también al reconocimiento de la importancia de la diversidad en las ideas y métodos científicos. Su historia sigue siendo un ejemplo poderoso de las dificultades y las recompensas de ser un pionero en un campo científico. En la siguiente parte de este artículo, exploraremos más sobre cómo su trabajo continúa influyendo en la genética moderna y otros campos científicos.
El Impacto Duradero de los Elementos Transponibles
El descubrimiento de los elementos transponibles por Barbara McClintock no solo fue un hito en la genética, sino que también ha tenido repercusiones profundas y duraderas en diversos campos de la biología. Estos elementos, a menudo denominados "genes saltarines", son secuencias de ADN que pueden cambiar de posición dentro del genoma, un proceso que puede alterar la función genética y generar variabilidad.
La idea de que el genoma no es una estructura estática, sino que está en constante flujo y cambio, fue una propuesta revolucionaria que ha transformado el entendimiento de muchos procesos biológicos. Este concepto básico permite explicar fenómenos como las mutaciones, que pueden desencadenar enfermedades genéticas, o incluso actuar como un motor de la evolución al introducir variabilidad genética en una población.
Los trabajos posteriores sobre elementos transponibles han revelado su presencia en casi todos los organismos vivos, desde bacterias hasta seres humanos. Se estima que aproximadamente el 50% del genoma humano está compuesto por secuencias derivadas de transposones, lo que subraya su importancia evolutiva y funcional. Estos elementos han sido implicados en la regulación de la expresión génica y el desarrollo de ciertos tipos de cáncer, lo que sitúa la obra de McClintock en el corazón de importantes investigaciones médicas actuales.
Desafíos y Reconocimientos a lo Largo del Camino
El camino hacia el reconocimiento de los descubrimientos de McClintock fue arduo y plagado de desafíos. En su tiempo, el mundo académico estaba dominado por hombres, y las mujeres como McClintock a menudo enfrentaban discriminación y escepticismo. Su enfoque innovador también chocó con la mentalidad conservadora de muchos científicos de la época, que estaban incrédulos ante la idea de un genoma dinámico.
Sin embargo, McClintock nunca permitió que estos obstáculos frenaran su entusiasmo por la ciencia. Continuó trabajando con dedicación, sin buscar constantemente la aprobación externa que a menudo se les niega a las mentes innovadoras en su tiempo. Su capacidad para superar la resistencia de sus colegas y seguir avanzando en su trabajo es un testimonio de su tenacidad y pasión por la investigación.
Aunque fue en los años 80 cuando finalmente recibió reconocimiento generalizado con el Premio Nobel, McClintock ya había recibido diversos galardones que indicaban el valor de sus contribuciones, como la Medalla Nacional de Ciencia de Estados Unidos en 1971. Estos honores subrayaban su estatus como una de las científicas más influyentes del siglo XX.
La Herencia de McClintock: Inspiración para Nuevas Generaciones
La historia de Barbara McClintock ha sido una fuente de inspiración para innumerables científicos jóvenes, especialmente mujeres, que buscan seguir sus pasos en la búsqueda del conocimiento. Su trabajo ejemplifica cómo la curiosidad y el coraje pueden desafiar las barreras establecidas, transformando conceptos fundamentales en ciencia y abriendo nuevas vías de investigación.
Más allá de su legado científico, la historia de su persistencia y determinación sirve como recordatorio poderoso de que las grandes ideas a menudo enfrentan oposición antes de ser aceptadas. Este desafío inherente en el descubrimiento científico resuena fuertemente con investigadores que hoy en día se enfrentan a retos similares en la búsqueda de nuevas verdades y entendimientos.
Para las mujeres en ciencia, McClintock representa un icono de éxito alcanzado con pasión y compromiso, al tiempo que lucharon contra la discriminación de género. Su vida y carrera son un recordatorio de que el talento y la dedicación pueden superar incluso los prejuicios más arraigados, brindando a las futuras generaciones un camino a seguir.
El Futuro de la Investigación en Genética
A medida que la tecnología avanza, el estudio de los elementos transponibles y la estructura dinámica del genoma sigue siendo un campo activo y vibrante de la investigación genética. Con herramientas modernas como la secuenciación de ADN de alto rendimiento, los científicos pueden explorar genomas completos con una profundidad que McClintock solo podría haber imaginado.
Estas innovaciones están llevando a descubrimientos que continúan ampliando nuestra comprensión de las funciones biológicas y su influencia en la salud y las enfermedades humanas. La investigación sobre transposones, por ejemplo, está ayudando a desentrañar los misterios detrás de la regulación genómica y la inestabilidad que puede llevar al desarrollo de diversas patologías.
En la siguiente parte de este artículo, exploraremos cómo los conceptos introducidos por Barbara McClintock están siendo utilizados en aplicaciones prácticas y teóricas en la genética moderna, y cómo su legado inspira a un nuevo siglo de científicos.
Aplicaciones Modernas de los Elementos Transponibles
Hoy en día, el estudio de los elementos transponibles, inicialmente revelado por Barbara McClintock, ha encontrado un lugar prominente en múltiples ámbitos científicos. Estas secuencias móviles de ADN no solo han resuelto enigmas fundamentales sobre variabilidad genética y evolución, sino que también han abierto vías para innovaciones tecnológicas y médicas.
Una aplicación significativa de los transposones se encuentra en la biotecnología y la ingeniería genética. Debido a su capacidad para insertar material genético en diferentes lugares del genoma, los transposones han sido utilizados como herramientas para desarrollar técnicas de mutagénesis y terapia génica. Esta última busca corregir defectos genéticos al introducir secuencias normales de ADN en células enfermas, abriendo así la posibilidad de tratar enfermedades genéticas hereditarias y ciertos tipos de cáncer.
En la agricultura, el conocimiento de estos elementos ha permitido avances en el cultivo de maíz y otros cereales, mejorando la resistencia a enfermedades y estrés ambiental. Los investigadores pueden manipular transposones para mejorar las características deseables en plantas, como la producción de cultivos más nutritivos o resistentes, de forma más rápida y eficiente que las técnicas de cría tradicionales.
La Influencia de McClintock en la Investigación Actual
El trabajo de Barbara McClintock no solo ha tenido implicaciones prácticas, sino que también ha influenciado cómo los científicos piensan acerca de la estructura y función del genoma. Sus descubrimientos enfatizaron la importancia de entender el genoma como una entidad activa y dinámica, lo que ha inspirado estudios en epigenética. Este campo investiga cómo las modificaciones químicas en el ADN, y no solo la secuencia de nucleótidos, pueden influir en la actividad genética y ser heredadas por las siguientes generaciones.
Con la creciente accesibilidad a tecnologías de secuenciación de próxima generación, los científicos están capacitados para investigar patrones epigenéticos complejos y oscilaciones genómicas a una escala sin precedentes. Esto ha brindado una nueva comprensión sobre el papel de los transposones en la regulación génica, el desarrollo embrionario y la adaptación evolutiva.
Además, los elementos transponibles proporcionan un modelo para estudiar la plasticidad genómica, un tema que está cobrando importancia en la comprensión de la adaptación de los organismos a un ambiente en constante cambio. Al reconocer que los genomas no son estables sino maleables, la investigación actual busca aplicar estos principios a áreas como la conservación de especies y la respuesta a desafíos ambientales globales.
Reflexionando sobre el Legado de Barbara McClintock
El impacto del trabajo de Barbara McClintock se extiende más allá del descubrimiento científico; cambia la forma en que valoramos y promovemos la diversidad de ideas en la ciencia. Su habilidad para desafiar convenciones científicas y perseverar frente a la resistencia institucional continúa inspirando a investigadores de todas las disciplinas para abordar problemas con una mentalidad aventurera y crítica.
El legado de McClintock es también un recordatorio de la trascendencia de las contribuciones individuales en un mundo científico dominado por el trabajo en equipo y la colaboración interdisciplinaria. Aunque trabajó en gran medida de manera independiente, su investigación ha servido de base crucial para innumerables estudios colaborativos que desarrollan aún más nuestras comprensiones genéticas.
Conclusión: Un Farol en la Ciencia Genética
Barbara McClintock, con su dedicación inigualable, perspicacia innovadora y resiliencia en el campo de la genética, permanece como un farol que ilumina el camino para futuras generaciones de científicos. Su enfoque visionario y su capacidad para enfrentarse a la resistencia con creatividad y coraje continúan siendo enseñanzas valiosas en la eterna búsqueda del conocimiento.
Aunque la comunidad científica del pasado tardó en reconocer la magnitud de sus descubrimientos, el reconocimiento otorgado a McClintock en sus últimos años ha asegurado que su legado perdure. A través de su trabajo pionero, no solo enriqueció nuestra comprensión de la genética, sino que también personificó el poder de la ciencia para desafiar las nociones establecidas y abrir nuevas fronteras para la humanidad.
En última instancia, el trabajo y la vida de Barbara McClintock resuenan como un testimonio de la perseverancia y la curiosidad que impulsan la frontera científica hacia adelante, inspirando un futuro lleno de descubrimientos y avances sin precedentes.


Frederick Sanger : Un Pionnier de la Génétique Moderne
Introduction
Dans l'impressionnant panthéon des scientifiques qui ont façonné notre compréhension moderne de la biologie, rares sont ceux qui se distinguent autant que Frederick Sanger. Connu pour ses réalisations révolutionnaires en biochimie et en génétique, Sanger a marqué l'histoire grâce à ses découvertes fondamentales dans le séquençage des acides nucléiques. Avec non pas une, mais deux Prix Nobel de Chimie à son actif, son impact sur la science moderne est incommensurable. Cet article se penche sur la vie, les découvertes et l'héritage d'un homme dont les contributions ont bouleversé notre compréhension du vivant.
Une Carrière Scientifique Précoce
Frederick Sanger est né le 13 août 1918 à Rendcomb, en Angleterre, dans une famille de quakers. Cette éducation non conformiste a sans doute influencé sa méthode de pensée indépendante et sa détermination. Très jeune, Sanger a montré un intérêt marqué pour les sciences naturelles, un intérêt encouragé par son père, un médecin généraliste. Après sa scolarité locale, il rejoint le St John's College de l'Université de Cambridge pour étudier les sciences naturelles. C'est là qu'il découvre sa passion pour la biochimie, une discipline alors en plein essor.
Pendant ses études de doctorat, Sanger travaille sous la direction de A.C. Chibnall, étudiant le métabolisme de l'azote chez les plantes. Ce projet lui a permis d'acquérir des compétences essentielles en techniques de séparation et d'analyse chimique. Toutefois, c'est en rejoignant le laboratoire de Charles Harington, où il se concentre sur l'insuline, que Sanger a véritablement trouvé sa voie.
Le Séquençage des Protéines
Frederick Sanger est surtout connu pour sa méthode de séquençage des protéines, un travail qui lui a valu son premier Prix Nobel de Chimie en 1958. À l'époque, la structure des protéines, bien que reconnue comme complexe, était peu comprise. Sanger a choisi de travailler sur l'insuline, une hormone peptidique, en grande partie à cause de sa relative simplicité structurelle et de sa disponibilité.
Utilisant des techniques de chromatographie sur papier et d'électrophorèse, il a déterminé la séquence complète des acides aminés de l'insuline bovine. Cette réalisation a imposé un standard pour l'analyse des protéines, démontrant qu'il était possible de déchiffrer la structure des molécules biologiques les plus complexes. L'approche méthodique et la persévérance de Sanger ont transformé un rêve scientifique en réalité, ouvrant la voie à une compréhension plus approfondie de la biologie moléculaire.
Les Bases du Séquençage de l'ADN
Après sa première grande percée, Sanger oriente ses recherches vers le séquençage des acides nucléiques. C'était un domaine encore plus ambitieux, mais Sanger, avec sa perspicacité inébranlable, s'y attèle avec détermination. En 1975, Sanger et son équipe développent une méthode révolutionnaire pour séquencer l'ADN, connue aujourd'hui sous le nom de méthode de terminaison de chaîne ou méthode Sanger.
Cette technique ingénieuse utilise des didésoxyribonucléotides pour interrompre l'élongation de l'ADN lors de la réplication, permettant ainsi de déterminer l'ordre des bases dans une séquence d'ADN. Elle a non seulement transformé le paysage de la biologie moléculaire, mais elle a aussi jeté les bases pour le développement de projets génomiques d'une ampleur inimaginable à l'époque, comme le Projet génome humain.
Un Deuxième Prix Nobel
En reconnaissance de son impact monumental sur notre compréhension des mécanismes génétiques, Frederick Sanger a reçu un second Prix Nobel de Chimie en 1980, une distinction qu'il partage avec Paul Berg et Walter Gilbert. Sanger est ainsi l'un des rares scientifiques à avoir été honoré par deux Prix Nobel dans la même discipline, soulignant l'importance capitale de ses contributions. Son travail n'a pas seulement ouvert de nouvelles avenues de recherche ; il a fondamentalement redéfini ce qui était possible en biochimie et en génétique.
L'héritage de Frederick Sanger perdure à travers ses contributions qui ont transformé la science moderne. Ses méthodes de séquençage sont aujourd'hui intégrées dans de nombreuses applications scientifiques et médicales, de la recherche en biologie fondamentale aux thérapies géniques personnalisées. Au-delà de ses innovations techniques, Sanger est souvent célébré pour son esprit curieux et sa volonté de défier les limites de la connaissance, des qualités qui inspirent encore les scientifiques du monde entier.
Impact sur la Recherche Biomédicale
Le travail pionnier de Frederick Sanger a eu un impact considérable sur la recherche biomédicale, influençant de nombreux domaines allant de la génétique des maladies à la pharmacologie. Avec l'essor des techniques de séquençage d'ADN, il est devenu possible d'identifier les mutations génétiques responsables de maladies héréditaires, ce qui a permis de mieux comprendre la pathologie de ces conditions et de développer de nouvelles approches thérapeutiques.
La méthode de séquençage de Sanger a été utilisée pour découvrir le code génétique sous-jacent à plusieurs maladies, comme la mucoviscidose, la maladie de Huntington, et bien d'autres encore. Cette capacité à lire le "livre de la vie" a permis aux scientifiques d'intensifier la recherche sur les bases génétiques des maladies complexes et de jeter les bases de la médecine personnalisée.
Vers la Médecine Personnalisée
Dans le contexte de la médecine personnalisée, l'héritage de Sanger est indéniable. La médecine personnalisée repose sur l'idée que les traitements médicaux peuvent être adaptés individuellement en fonction du profil génomique d'un patient. Cette approche permet non seulement un traitement plus efficace, mais elle réduit également le risque d'effets secondaires, en optimisant le choix des médicaments et leurs dosages spécifiques à chaque individu.
La capacité à séquencer et à analyser le génome individuel, rendue possible par les percées de Sanger, a révolutionné la manière dont les médecins abordent le traitement des maladies. Aujourd'hui, il est courant que les oncologues utilisent le séquençage génomique pour identifier des mutations spécifiques dans les tumeurs afin de prescrire des thérapies ciblées. Ces avancées démontrent comment les fondations posées par Sanger continuent à transformer le paysage des soins de santé, apportant des bénéfices tangibles aux patients du monde entier.
L'Évolution des Techniques de Séquençage
Bien que la méthode de terminaison de chaîne de Sanger ait dominé le séquençage d'ADN pendant plusieurs décennies, les avancées technologiques ont depuis introduit de nouvelles méthodes qui permettent un séquençage plus rapide et plus économique. Cependant, la méthodologie de Sanger reste une référence fiable et est encore utilisée dans de nombreux laboratoires pour des travaux nécessitant une précision et une exactitude élevées.
Les nouvelles technologies, telles que le séquençage à haut débit, ont permis d'analyser simultanément des millions de fragments d'ADN, réduisant considérablement le temps et le coût des projets de séquençage. Ces progrès ont rendu possible des initiatives ambitieuses comme le Projet génome humain, qui a cherché à séquencer et à cartographier tous les gènes du génome humain. Il est essentiel de reconnaître que, sans les innovations fondamentales apportées par Sanger, ces progrès modernes n'auraient peut-être jamais vu le jour.
Un Héritage Éducatif et Inspirant
Au-delà de ses contributions techniques, Frederick Sanger a inspiré d'innombrables scientifiques à travers le monde. Connu pour sa modestie et son approche collaborative du travail scientifique, il a toujours mis l'accent sur l'importance de la recherche fondamentale, même lorsque ses applications pratiques n'étaient pas immédiatement apparentes. Cette philosophie a encouragé un environnement de recherche où l'exploration scientifique est valorisée pour son potentiel à élargir notre compréhension collective.
De nombreux chercheurs contemporains, ayant bénéficié directement des innovations de Sanger, témoignent de son influence dans leur formation académique et professionnelle. Ses travaux ne sont pas seulement inscrits dans les manuels scientifiques, mais ils sont également intégrés dans les pratiques de laboratoire, formant la prochaine génération de biologistes et de généticiens.
Conclusion
Frederick Sanger, avec ses innovations qui ont changé le cours de la science, reste une figure incontournable dans l'histoire de la biochimie et de la génétique. Ses découvertes, ayant conduit à une multitude de progrès dans la compréhension des mécanismes moléculaires, continueront d'inspirer et d'influencer les générations futures. Alors que la science avance à un rythme effréné, l'héritage de Sanger nous rappelle l'importance d'une recherche méthodique, de la rigueur intellectuelle et de l'inventivité. Son travail exemplaire souligne la puissance des découvertes fondamentales qui, lorsqu'elles sont réalisées, possèdent le potentiel d'impacter positivement notre monde de manière durable.
Défis et Éthique du Séquençage Génétique
Alors que le séquençage génétique, initié en grande partie grâce aux travaux de Frederick Sanger, a ouvert de vastes horizons dans le domaine scientifique et médical, il a également soulevé des questions éthiques et sociales complexes. La capacité à décoder le génome humain soulève des préoccupations concernant la confidentialité des données génétiques, le consentement éclairé, et l'utilisation potentielle de ces informations par les assureurs ou les employeurs.
Les dilemmes éthiques incluent aussi la question de savoir qui devrait avoir accès à ces informations et dans quelles conditions. Le génome d'une personne contient non seulement des informations essentielles sur sa santé actuelle, mais peut aussi révéler des prédispositions à des maladies futures, posant des questions sur le droit de ne pas savoir et les implications pour la famille et la communauté élargie.
L'Avenir de la Génétique
À mesure que la science progresse, l'application des séquençages génétiques ne cesse de s'élargir. Les chercheurs continuent d'affiner et d'innover les techniques, rendant le séquençage toujours plus rapide et accessible. Des technologies comme CRISPR-Cas9, qui permettent l'édition précise du génome, ont vu le jour, ouvrant des possibilités inimaginables pour le traitement des maladies génétiques et les améliorations biotechnologiques.
Elles soulèvent cependant la nécessité d'un débat global et informé sur les implications éthiques et sociétales. Le potentiel de ces technologies est énorme : de l'éradication des maladies héréditaires à la modification des caractéristiques humaines. Toutefois, il est crucial de naviguer prudemment, en établissant des cadres législatifs et éthiques adéquats pour guider l'usage de ces puissantes technologies.
Reconnaissance et Hommages
Frederick Sanger a non seulement transformé le domaine scientifique par ses découvertes, mais sa vie et son travail sont souvent cités comme des exemples d'intégrité et d'humilité en recherche. Après sa retraite officielle, il a continué d'interagir avec le monde scientifique, bien qu'il mène une vie relativement discrète, préférant se consacrer à des passions personnelles comme le jardinage.
De nombreuses institutions ont honoré Sanger en nommant des centres de recherche à son nom. Notamment, le Wellcome Sanger Institute, fondé en 1992, joue un rôle clé dans le Projet génome humain et continue de mener des recherches de pointe en génomique. Ces hommages témoignent de l'empreinte indélébile qu'il a laissée sur la communauté scientifique mondiale.
Influence Pédagogique
Frederick Sanger a influencé des générations de scientifiques non seulement par ses découvertes, mais aussi par son approche de l'éducation et de la formation. Malgré ses deux Prix Nobel, il est resté profondément attaché à l'idée de transmettre le goût de l'exploration et de la rigueur méthodique aux jeunes chercheurs. Nombre de ses étudiants et collaborateurs soulignent l'importance de ses méthodes de travail méticuleuses et de son esprit d'innovation.
Cette passion pour l'éducation a également permis d'établir des programmes universitaires qui adoptent une approche interdisciplinaire, intégrant la biochimie, la biologie moléculaire et la génétique. Ainsi, Sanger a indirectement influencé la manière dont la science est enseignée, en favorisant une approche intégrée et collaborative de la recherche.
Conclusion: Un Héritage Durable
Le parcours exceptionnel de Frederick Sanger est un testament à la puissance de la curiosité scientifique et de la persévérance. Ses réalisations ont non seulement façonné notre compréhension actuelle de la biologie moléculaire, mais elles continuent d'inspirer des innovations qui pourraient transformer la science et la médecine pour les décennies à venir. Dans un monde de plus en plus technologique, l'œuvre de Sanger nous rappelle l'importance de la recherche fondamentale et des implications éthiques de nos découvertes.
Son héritage ne se limite pas aux technologies qu'il a développées ; il incarne également une philosophie de la créativité scientifique, du respect de la vérité et du potentiel humain. Alors que nous continuons à explorer de nouvelles frontières en génétique et en biotechnologie, la vie et l'œuvre de Frederick Sanger resteront des balises guidant les générations futures vers des découvertes révolutionnaires tout en respectant les principes éthiques fondamentaux.
Friedrich Miescher: El Pionero Desconocido del ADN
El nombre de Friedrich Miescher puede no ser tan reconocido como debería en el ámbito público, sin embargo, su contribución a la ciencia ha sido crucial para uno de los mayores descubrimientos en la biología moderna: el ácido desoxirribonucleico, conocido mundialmente por sus siglas como ADN. Esta molécula es el libro de instrucciones para la vida, y fue Miescher quien primero la identificó, estableciendo las bases para un campo de estudio que ha revolucionado la medicina, la genética y tantas otras disciplinas científicas.
El Comienzo de una Carrera Científica
Friedrich Miescher nació el 13 de agosto de 1844 en Basilea, Suiza, en el seno de una familia con un fuerte legado en el campo de las ciencias y la medicina. Su padre, Jakob Miescher, era un médico prominente, lo que probablemente influyó en su decisión de seguir una carrera en el campo de la medicina. Miescher comenzó sus estudios universitarios en medicina en la Universidad de Basilea y más tarde continuó en la Universidad de Gotinga, donde se graduó en 1868.
Su interés por la investigación se manifestó pronto, llevándolo a realizar estudios de posgrado bajo la dirección de Felix Hoppe-Seyler, un pionero en el estudio de la fisiología y la bioquímica. Hoppe-Seyler dirigía un laboratorio en Tubinga, Alemania, conocido por su enfoque en la química fisiológica, un campo novedoso en la época. Fue en este laboratorio humilde y a menudo en condiciones improvisadas, donde Miescher haría su descubrimiento más importante.
El Descubrimiento de la Nucleína
En su investigación inicial, Miescher se centró en el estudio de los glóbulos blancos extraídos de vendas quirúrgicas saturadas de pus. A través de métodos laboriosos de separación química, logró aislar una sustancia hasta entonces desconocida y diametralmente diferente a las proteínas y otros componentes celulares típicos. Este material, que era resistente a la absorción de agua y contenía elevados niveles de fósforo, lo llamó "nucleína".
La nucleína no resultaba ser un simple hallazgo de interés académico. Era algo revolucionario, aunque Miescher era inicialmente cauto sobre su significado debido a la falta de herramientas para analizar profundamente su estructura. Su naturaleza diferente a lo conocido insinuaba que podía haber funciones celulares más importantes y complejas de lo que se pensaba hasta entonces. Aunque él no se percató de inmediato, la nucleína se establecería más adelante como el ADN.
Impacto Inicial y Reconocimientos
A pesar del descubrimiento de Miescher, no fue hasta varias décadas después que la importancia de la nucleína, posteriormente reconocida como ADN, comenzó a ser plenamente entendida. En el momento de su descubrimiento, la comunidad científica todavía estaba fuertemente enfocada en las proteínas como las principales moléculas de la herencia, debido a su diversidad y complejidad estructural.
El trabajo de Miescher no ganó el reconocimiento inmediato en su época, pero estableció una base crucial sobre la cual se erigirían futuros descubrimientos científicos. Incluso durante su vida, siguió explorando áreas relacionadas, como los mecanismos de respiración en los tejidos, pero fue su interés por las biomoléculas lo que eventualmente le aseguró un lugar en la historia científica.
Experiencias Personales y Errores de Interpretación
A lo largo de su carrera, Miescher se encontró con varios desafíos, no solo técnicos sino también personales. La reticencia del entorno académico de la época a aceptar la relevancia de su hallazgo en ocasiones lo desembocaba en dudas. Además, su salud fue frágil; Miescher padecía de tuberculosis, una enfermedad que en última instancia acortaría su vida a la edad de 51 años, en 1895.
Un aspecto fascinante del trabajo de Miescher fue su constante intento por interpretar el significado biológico de su descubrimiento en un contexto más amplio. Aunque al principio sus teorías sobre el papel del ADN no eran correctas, proporcionaron una plataforma para discusiones y exploraciones futuras que, con el tiempo, resultaron críticas para avanzar en nuestra comprensión actual del material genético.
Legado Científico
El legado de Friedrich Miescher es monumental, pese a que durante mucho tiempo permaneció bajo las sombras de otros científicos. Fue a mediados del siglo XX que el papel esencial del ADN en la genética comenzó a ser plenamente comprendido, especialmente con los trabajos de James Watson y Francis Crick, quienes determinaron la estructura de doble hélice del ADN en 1953. Sin embrago, fue el trabajo pionero de Miescher que marcó el inicio de este viaje científico hacia la elucidación de los mecanismos de la vida al nivel molecular.
Miescher puede no haber llegado a comprender la importancia total de su descubrimiento dentro de su vida, pero su perseverancia y dedicación a la investigación científica sentaron precedentes para un siglo de avance en la biología molecular y la genética.
Evolución del Entendimiento del ADN
Aunque inicialmente el descubrimiento de la nucleína no recibió la atención esperada, Miescher había abierto las puertas para que futuros científicos profundizaran en el misterio del material genético. La historia del ADN es en realidad una serie de pasos incrementales, cada uno apoyándose en hallazgos previos, y Miescher es considerado la primera figura en este largo viaje.
En las décadas posteriores al descubrimiento de Miescher, científicos de todo el mundo emprendieron métodos más avanzados para comprender la composición química y posible función del ADN. Por ejemplo, en la década de 1920, Phoebus Levene identificó los componentes básicos del ADN: los nucleótidos. Sin embargo, las propiedades exactas y, más importante aún, el rol del ADN en la herencia continuaron siendo un misterio.
El punto de inflexión llegó en 1944, cuando Oswald Avery, Colin MacLeod y Maclyn McCarty demostraron que el ADN era el portador del material hereditario, un descubrimiento que cimentó el reconocimiento de Miescher como el pionero de este campo. Luego, en 1952, las famosas imágenes de difracción de rayos X de Rosalind Franklin y Maurice Wilkins proporcionaron pistas cruciales sobre la estructura de la molécula, un logro que culminó en el modelo de doble hélice propuesto por Watson y Crick.
Friedrich Miescher: Reconocimiento Tardío
Poco se habla en los textos introductorios sobre la importante contribución de Miescher, y es que, a menudo, las historias científicas tienden a celebrar aquellos descubrimientos que tienen un impacto inmediato y transformador. Sin embargo, figuras como Miescher son recordatorios de las raíces modestamente iniciadas de descubrimientos que luego llegan a cambiar el curso de la historia científica.
Con el tiempo, el campo de la biología molecular se organizó alrededor del ADN, y el redescubrimiento de los trabajos de Miescher posicionó a Suiza como un lugar significativo en la historia de la genética. La Universidad de Tubinga, donde llevó a cabo sus experimentos, ha sido reconocida como un sitio de interés histórico-científico debido a su trabajo pionero.
En la actualidad, Miescher es recordado no solo como el hombre que descubrió la nucleína, sino como el padre de la biología molecular moderna. Muchas instituciones y programas de biología llevan su nombre en reconocimiento a su contribución. Así, aunque su reconocimiento llegó tarde, su legado influye diariamente en investigaciones relacionadas con la genética y la biología.
Pionero de la Ciencia Interdisciplinaria
El enfoque de Friedrich Miescher en su investigación es un ejemplo temprano de la ciencia interdisciplinaria. Durante su tiempo, la bioquímica y la biología todavía estaban estableciendo sus identidades como disciplinas científicas separadas. Sin embargo, Miescher exploró campos que más tarde se convertirían en componentes cruciales de la biología molecular. La simple elección de usar soluciones químicas para aislar compuestos de los glóbulos blancos fue, en sí misma, una aplicación interdisciplinaria que combinaba química con biología celular.
Miescher no solo trataba de comprender la estructura y función del ADN, sino que también estaba muy interesado en cómo las distintas moléculas dentro de las células contribuían a procesos vitales como la respiración. Este enfoque multifacético fue un precursor de cómo se hace ciencia en tiempos modernos, donde entender problemas complejos requiere la colaboración de distintas disciplinas científicas.
El Impacto del ADN en la Ciencia Moderna y su Influencia Universal
La importancia del descubrimiento de Miescher se ha magnificado a lo largo de los años con el advenimiento de nuevas tecnologías y métodos científicos. En particular, la capacidad de secuenciar el ADN ha sido revolucionaria; ha permitido a los científicos comprender las bases moleculares de la herencia, enfermedades genéticas, y la biodiversidad.
En medicina, la identificación de genes relacionados con enfermedades ha llevado a la creación de terapias dirigidas y personalizadas. La genómica, que investiga la estructura, función y evolución de los genomas, ha transformado nuestro entendimiento de una vasta gama de condiciones y trastornos humanos.
Además, la biotecnología ha desbloqueado aplicaciones prácticas del ADN en numerosas industrias, desde la agricultura hasta la farmacología. Gracias a esto, el trabajo preliminar de patentados científicos como Friedrich Miescher ha incrementado el potencial de investigación colaborativa global, rompiendo barreras científicas a lo largo de los continentes.
Friedrich Miescher, aunque no tuvo la oportunidad de ver el impacto final de su descubrimiento, estableció un pilar en el fascinante y vasto campo del estudio del material hereditario. Su vida y obra permanecen como testimonios de la ciencia tenaz y aventurera que desafía las probabilidades y expande el conocimiento humano en formas que sus primeros descubridores a menudo no pueden imaginar.
La Ética y las Implicaciones Futuras del ADN
A medida que avanzamos en el siglo XXI, el legado del descubrimiento de Friedrich Miescher se extiende más allá de las fronteras puramente científicas para abarcar también cuestiones éticas y sociales. La facilidad con la que hoy se puede manipular el ADN plantea preguntas significativas sobre los límites éticos de su uso.
La edición genética, posibilitada por tecnologías como CRISPR-Cas9, permite realizar cambios precisos en el genoma. Esto abre prometedoras vías para la corrección de enfermedades genéticas, pero también plantea dilemas sobre la modificación genética en humanos. Estos avances nos enfrentan a preguntas sobre la naturaleza de la herencia, la selección genética y el potencial para crear desigualdades biológicas.
El trabajo de Miescher, aunque inocente en su tiempo, plantó las semillas de una revolución que requiere un manejo responsable y ético. Cuestiones sobre quién debería tener acceso a las tecnologías genéticas, cómo proteger la privacidad genética de los individuos y de qué manera el conocimiento derivado del ADN podría ser mal usado, permanecen activas en el debate científico y social contemporáneo.
Fomentando el Conocimiento Científico
Hay un continuo esfuerzo por educar al público sobre la importancia del ADN y sus aplicaciones. Esto no es solo un desafío para transmitir información técnica, sino también para aumentar la comprensión de por qué estos desarrollos son relevantes para la sociedad en su conjunto.
Iniciativas educativas y programas de divulgación buscan inspirar a futuras generaciones de científicos, usando la historia de Miescher como un ejemplo de cómo la curiosidad y la determinación pueden conducir a descubrimientos que cambian el mundo. Los museos de ciencias, exposiciones itinerantes y plataformas educativas en línea juegan un papel crucial en este proceso. Celebrar el legado de Miescher y generar interés en su visión es clave para fomentar una sociedad que valore el progreso científico basado en la ética.
Reflexiones sobre Friedrich Miescher
Hoy celebramos a Friedrich Miescher no solo por sus descubrimientos científicos, sino también como un símbolo de perseverancia e inspiración científica. Su vida ilustra el impacto de los logros muchas veces invisibles que mueven el mundo hacia adelante. Sus éxitos nos recuerdan que frecuentemente los grandes descubrimientos provienen del trabajo arduo y dedicado realizado lejos de los reflectores.
La historia de Miescher también es un reflejo de cómo nuestras percepciones sobre lo que es importante en la ciencia pueden cambiar con el tiempo. A medida que nuestra capacidad técnica y nuestro entendimiento continúan evolucionando, nuevos aspectos de su trabajo emergen, demostrando una relevancia que crece a través de las décadas.
Mientras la ciencia sigue avanzando con descubrimientos que aún no podemos imaginar completamente, el caso de Miescher enseña que los cimientos del futuro siempre han sido impulsados por esfuerzos humildes e inquebrantables de aquellos que se dedican a explorar lo desconocido.
Friedrich Miescher sigue resonando en los pasillos de la historia de la ciencia. Desde su labor en un pequeño laboratorio en Tubinga, su legado ha expandido nuestros horizontes hacia un futuro más profundo y significativo en el ámbito de la genética y más allá, asegurándose que su postergado reconocimiento se traduzca en eterno respeto y admiración.







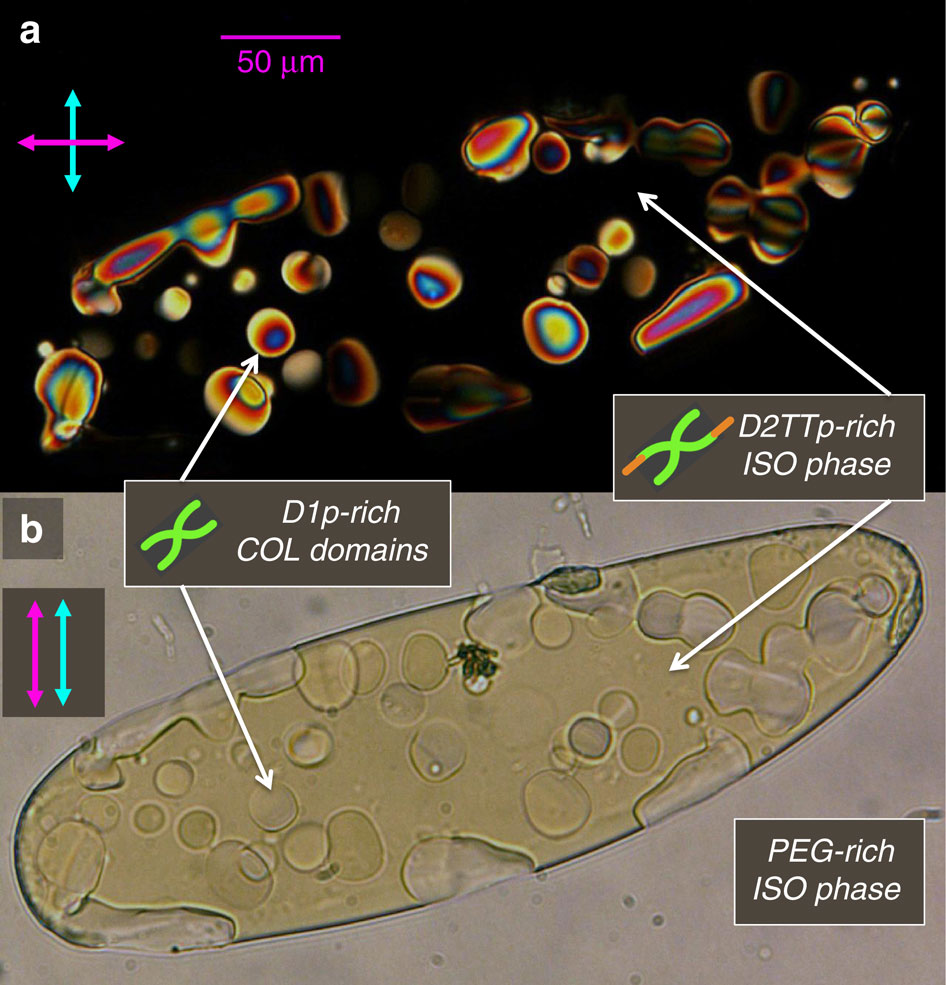


:quality(70)/cloudfront-eu-central-1.images.arcpublishing.com/liberation/4AWJSVQKY2ITPGLX5KLHJYREV4.jpg)

